
题目列表(包括答案和解析)
20.(8分)某学生用标准的0.2mol/L的盐酸滴定待测的NaOH溶液,其实验操作如下:
A.用碱式滴定管取待测液NaOH溶液放入锥形瓶,滴加2-3滴酚酞指示剂。
B.用待测的NaOH溶液润洗碱式滴定管。
C.把滴定管用蒸镏水洗净。
D.取下酸式滴定管,用标准的盐酸溶液润洗后,再将标准的盐酸注入酸式滴定管至刻
度“0”以上2cm-3cm处,把酸式滴定管固定好,调节液面。
E.检查滴定管是否漏水,并分别固定在滴定管架两边。
F.另取锥形瓶,再重复滴定操作一次。
G.把锥形瓶放在酸式滴定管的下面,瓶下垫一张白纸,然后边滴定边摇动锥形瓶,直
至终点,记下滴定管的液面所在刻度。
据上述滴定操作,完成下列填空:
①滴定操作的正确操作顺序是(用上述各编号字母填写)
→E→ →B→ → → ;
②G步操作中判断滴定终点的依据是 ;
③D步骤的操作中液面应调节到 ,尖嘴部分应 ;
④酸式滴定管未用标准的盐酸润洗,待测溶液NaOH的测定值会 ;碱式滴定管
未用待测的NaOH溶液润洗,待测NaOH溶液的测定值会 。(填“偏高”、
“偏低”或“无影响”。)
 四、(本题包括3小题,共28分)
四、(本题包括3小题,共28分)
19.(5分)以试管和胶头滴管为仪器,用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制
的NaOH溶液反应制备白色的Fe(OH)2沉淀。
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入 。
②生成白色Fe(OH)2沉淀的操作是 ,
这样做的理由是 。
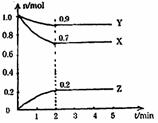
18.恒温下,在容积固定的密闭容器中充入1mol HI达到平衡时,I2(g)的体积分数为x。若再
向该容器中充入1mol HI并再次达到平衡时,I2(g)的体积分数为y,则x与y的大小关系
为 ( )
A.x>y B.x<y C.x =y D.无法判断
第Ⅱ卷(非选择题,共54分)
17. 在密闭容器中进行下列反应:M(g)+N(g) R(g)+2L此反应符合下列图象(R%为R
在密闭容器中进行下列反应:M(g)+N(g) R(g)+2L此反应符合下列图象(R%为R
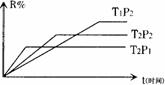 在平衡混合物中的体积分数),则该反应是 ( )
在平衡混合物中的体积分数),则该反应是 ( )
A.正反应是吸热反应,L是气体
B.正反应是放热反应,L是气体
C.正反应是吸热反应,L是固体
D.正反应是放热反应,L是固体或液体
16.将下列物质的溶液,加热蒸干并灼烧,能够得到原来物质的是 ( )
A.FeCl3 B.NaHCO3 C.硫酸镁 D.Na2CO3
15.在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中加入足量的Na2O2固体,充分反应后,再加
入过量的稀盐酸,完全反应后,离子数目没有变化的是 ( )
A.Fe3+ B.Fe2+ C.Al3+ D.NH4+
14.某溶液中加入铝片有氢气产生,则在该溶液中一定能够大量共存的离子组是 ( )
A.Cl-、NO3-、Ba2+、Na+ B.Na+、K+、SO42-、Cl-
C.NH4+、Ba2+、Cl-、HCO3- D.SO42-、CH3COO-、Al3+、Mg2+
13.向某溶液中加入含Fe2+的溶液后,无明显变化。当再加入几滴新制氯水后,混合液变成
红色,则下列结论中错误的是 ( )
A.该溶液中一定含SCN- B.氧化性:Fe3+>Cl2
C.Fe2+与SCN-不能形成红色物质 D.Fe2+被氯水氧化为Fe3+
12.容积固定为3L的某密闭容器中加入1molA、2molB,一定温度下发生如下反应:
 A(s)+2B(g)
C(g)+D(g),经反应5min后,测得C的浓度为0.3mol/L。下列说法中正
A(s)+2B(g)
C(g)+D(g),经反应5min后,测得C的浓度为0.3mol/L。下列说法中正
确的是 ( )
A.5min内D的平均反应速率为0.02mol·(L·min)-1
B.5min内B的平均反应速率为0.12mol·(L·min)-1
C.经5min后,向容器内再加入C,正反应速率变小
D.平衡状态时,生成1molD的同时生成1molA
11.能说明醋酸是弱电解质的是 ( )
A.醋酸钠溶液显碱性
B.用食醋可以除热水瓶内的水垢
C.pH=2的醋酸溶液稀释1000倍后pH小于5
D.用浓H2SO4和醋酸钠固体共热可制得醋酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com