
题目列表(包括答案和解析)
9. 将 a g 含NaOH的样品溶解在b mL 0.1 mol·L-1 的 H2SO4 中,再加入 c mL 0.1mol·L-1 的氢氧化钡溶液,反应后所得溶液恰好呈中性,则样品中NaOH的纯度是
A. [(b-c)/125a ]× 100% B. [(b-2c)/125a ]×100%
C. [(b-c)/250 a ] ×100 % D. [(8b-8c)/ a]× 100%
8. 现有物质的量浓度均为 0.1 mol·L - 1 的下列五种物质的溶液:①HCl ②H2SO4 ③ CH3COOH ④ NH4Cl ⑤ NaOH。其溶液中由水电离出的c(H +) 的大小关系是
A. ① = ②>③>④>⑤ B. ④>③>① = ⑤>②
C. ③>①>②>④>⑤ D. ④>③>①>⑤>②
7. 已知NaHSO4 在水中的电离方程式为:NaHSO4 = Na + + H + + SO2-4 。某温度下,向 pH = 6 的蒸馏水中加入NaHSO4 晶体,保持温度不变,测得溶液中的pH为 2 。对于该溶液,下列叙述不正确的是
A. 该温度高于25℃
B. 水电离出来的c(H +)=1×10 - 10 mol ·L-1
C. c(H +)= c(OH -)+ c(SO2-4 )
D. 该温度下加入等体积 pH为 12 的NaOH 溶液可使反应后的溶液恰好呈中性
6. 25℃时,某溶液中由水电离出的H+的浓度为1×10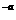 mol/L,下列说法正确的是
mol/L,下列说法正确的是
A.当a>7时,水的电离一定受到促进 B.当a<7时,水的电离一定受到抑制
C.当a>7时,溶液的pH为a或14-a D.当a<7时,溶液的pH为a或14-a
5. 在水溶液中能大量共存的离子组是
A. Na+ Fe3+ Cl- SCN- B. K + S2- SO2-4 H +
C. K + Al3+ Cl- AlO-2 D. Fe2+ Na+ NO-3 SO2-4
4. 下列事实不能用勒夏特列原理解释的是
A. 钢铁在潮湿的空气中容易生锈
B. 将FeCl3溶液加热蒸干最终得不到FeCl3固体
C. 实验室可用排饱和食盐水的方法收集氯气
D. 将滴有酚酞试液的Na2CO3溶液加热,溶液颜色加深
3. 在容积一定的密闭容器中存在如下反应:
在容积一定的密闭容器中存在如下反应:
A(g)+B(g) xC(g);生成物C的体积分数
xC(g);生成物C的体积分数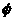 与外界条件温度、压强的关系如下图,相关的判断正确的是
与外界条件温度、压强的关系如下图,相关的判断正确的是
A.T1<T2 、P1>P2、a<0、x<3
B.T1>T2 、P1<P2、a>0、x>3
C.T1>T2 、P1<P2、a<0、x<3
D.T1>T2 、P1>P2、a>0、x<3
2. 体积相同的盐酸与醋酸,当c(Cl- ) = c(CH3COO - )时,则它们的
A. pH相同 B. 物质的量浓度相同
C. 吸收NH3 体积一样 D. 都稀释一倍后,c(Cl- )与c(CH3COO - ) 仍相同
1. 在含有酚酞的 0.1 mol/L 氨水中加入少量 NH4Cl 晶体,则溶液颜色
A. 变深 B. 变浅 C. 变蓝色 D. 不变
21. 在160mL未知浓度的稀硫酸中,加入100mL浓度为0.4mol/L的BaCl2溶液,生成白色沉淀,反应后H2SO4有剩余,尚需加入48mL浓度为2mol/L的NaOH溶液才能使溶液的pH为7,试计算:
(1)写出有关反应的化学反应方程式______________________________________ ___
(2)求白色沉淀BaSO4的质量(要写计算过程)
(3)原H2SO4溶液的物质的量浓度为多少?(要写计算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com