
题目列表(包括答案和解析)
30.化学平衡状态是指在一定条件下的______反应中,正反应和逆反应速率_______,反应混合物中各组分的百分含量保持________的状态。影响化学平衡的条件是_________,__________,_________。催化剂对平衡______影响。
29.化学反应速率是用来衡量化学反应进行快慢程度,通常用单位时间内反应物浓度的______ 或生成物浓度的______ 来表示。常用单位有_________ 。同一反应中各物质化学反应速率之比等于其化学方程式中
之比。影响化学反应速率的内因是_____________,外因是_________ ,___________ ,___________ 和____________ 。
26、根据烷、烯、炔烃燃烧的反应式,有人总结出以下规律:对于烷烃有n(烷烃)=n(H2O)-n(CO2),对于烯烃有n(H2O)-n(CO2)=0,对于炔烃有n(炔烃)=n(CO2)-n(H2O)。请回答下列问题:
 (1)某混合气体由C2H6和C3H4组成。将1.0体积混合气在氧气中充分燃烧,产生的CO2体积比水蒸气多0.2体积(相同状况下测定),通过计算确定C2H6和C3H4的体积。(设体积单位为升)
(1)某混合气体由C2H6和C3H4组成。将1.0体积混合气在氧气中充分燃烧,产生的CO2体积比水蒸气多0.2体积(相同状况下测定),通过计算确定C2H6和C3H4的体积。(设体积单位为升)
(2)某混合气由烯烃和烷烃或烯烃和炔烃组成。组成中可能是两种气体,也可能是多种气体。将1.0体积混合气在氧气中充分燃烧,产生3.0体积CO2和2.4体积水蒸气(相同状况下测定)。
①判断混合气体有________________两类烃组成。
②上述判断的理由是___________________________________________ _
(用简要文字叙述)。
③上述两类烃的体积比为__________________________。
25、能源是人类社会发展进步的物质基础。在当代,能源同信息、材料一起构成了现代文明的三大支柱。
(1)为了降低汽车尾气对大气的污染,北京市有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。请写出表示甲醇燃烧热的热化学方程式。
(2)测定工业甲醇中CH3OH的质量分数可按下法:取0.100g工业甲醇样品,以适量H2SO4酸化后,加入20.00mL 0.200mol/L的K2Cr2O7溶液,再用0.300mol/L FeSO4标准溶液滴定,耗去此标准液20.00mL时,刚好到达滴定终点。
已知:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与FeSO4溶液反应的离子方程式。
②求此工业甲醇中CH3OH的质量分数。
24、禽流感在全球的蔓延,使人们谈“禽”色变。从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物。

(1)达菲分子中含有的官能团有_______________________________________;
(2)莽草酸在浓硫酸作用下加热可以得到B(B的结构简式为: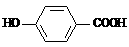 ),其反应类型为:_______________;
),其反应类型为:_______________;
(3)请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):
____________________________________________________________________;
(4)B的同分异构体中既含有酚羟基又含有酯基的共3种,写出其中一种同分异构体的结构简式______________________________。
23、已知 在光照条件下能够与氯气发生反应:
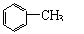
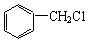 + Cl2
+ Cl2 + HCl
+ HCl
CH2=CHCH3+Cl2 CH2=CHCH2Cl+HCl
CH2=CHCH2Cl+HCl
现以原料A开始实现下列转化:
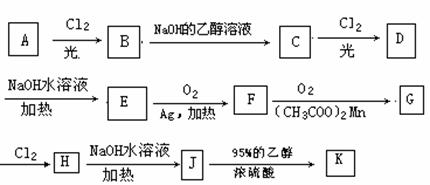
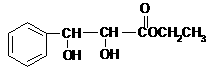
K的结构简式为: CH(OH)CH(OH)COOCH2CH3
CH(OH)CH(OH)COOCH2CH3
根据要求写出下列反应方程式
(1)A→B ;
(2)E→F ;
(3)H→J ;
整个过程中涉及到的反应类型有(按照反应进行的先后顺序)
。
22、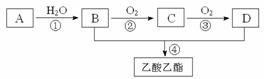 已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
回答下列问题:
(1)写出A的电子式 。
(2)A、B、C、D分子中能和金属钠反应的基团是 (填名称)。
(3)写出下列反应的反应类型:
① ,② ,④ 。
(4)写出下列反应的化学方程式:
① ;
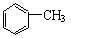 ②
。
②
。
21、铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
 Pb+PbO2+4H++2SO2-4
Pb+PbO2+4H++2SO2-4  2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是______________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加________g。
(2)在完全放电耗尽PbO2和Pb时,若按如图连接,电解一段时间后,则在A电极上生成__________、B电极上生成________,此时铅蓄电池的正负极的极性将___________。
20、Ⅰ.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇的试管里,反复操作几次。
请你评价若用上述方法制取乙醛存在哪些不足:_____________________。
 Ⅱ.课外活动小组甲,自行设计了下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去。请回答下列问题:
Ⅱ.课外活动小组甲,自行设计了下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去。请回答下列问题:
(1)实验前,首先检查装置的气密性,然后分别向试管A中加入乙醇,C中加入水;
(2)实验时,先加热B装置中的玻璃管,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。
①乙醇的催化氧化反应是________反应(填“放热”或“吸热”),该反应的化学方程式为___________________________________________________;
②通入空气的速度过快或过慢都不利于反应的进行,控制气体流速的实验操作现象是:_______________________________________________。
Ⅲ.课外活动小组乙,在研究了课外活动小组甲的方案后,认为该方案中有不足和不安全的地方。
(3)课外活动小组乙对甲的方案提出改进意见:
①将A装置浸在70-80℃的水浴中,目的是____________________;
②装置B、C之间接上丁装置,请你在上面方框中,画出D的装置图。
(4)如果在装置B、C之间不增加D装置,提出你对实验改进的意见:
____________ 。
19、实验室利用如右图装置进行中和热的测定。回答下列问题:
⑴该图中有两处未画出,它们是 、 ;
⑵在操作正确的前提下提高中和热测定的准确性的关键是: ;
⑶如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将 (填“偏大”、“偏小”、“不变”);原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com