
题目列表(包括答案和解析)
1.下列各组物质中,互为同分异构体的是( )
A.O2和O3 B. 11H和12H C. 甘氨酸和硝基乙烷 D.丙烷和丁烷
26.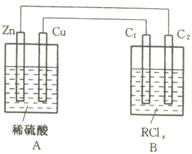 某金属R的氯化物RClx13.5g溶于水配成0.100 mol·L-1的水溶液1.00L。取该溶液放入下图的B烧杯中,电解一段时间,Cu极上放出11.2毫升(标准状况)气体,B烧杯中C2极的质量增加0.0320g。求金属R的相对原子质量。
某金属R的氯化物RClx13.5g溶于水配成0.100 mol·L-1的水溶液1.00L。取该溶液放入下图的B烧杯中,电解一段时间,Cu极上放出11.2毫升(标准状况)气体,B烧杯中C2极的质量增加0.0320g。求金属R的相对原子质量。
25.已知:(1)Fe2O3(s) + 3CO(g) == 2Fe(s) + 3CO2(g) △H1= -26.7kJ/mol
(2)3Fe2O3(s) + CO(g) == 2Fe3O4(s) + CO2(g) △H2= -50.75kJ/mol
(3) Fe3O4(s) + CO(g) == 3FeO(s) + CO2(g) △H3= -36.5kJ/mol
计算反应:2FeO(s) + 2CO(g) == 2Fe(s) + 2CO2(g)的△H 。
24.某同学查资料得知α-AgI是一种固体导体,导电率很高。他为了研究α-AgI究竟是Ag+离子导电还是I-离子导电,设计一个如图所示(用铅蓄电池做电源)的电化学实验。
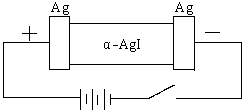
 已知铅蓄电池总反应:
已知铅蓄电池总反应:
Pb+PbO2+2H2SO4 2PbSO4+2H2O
(1)该电解池的阳极电极方程式:
;
铅蓄电池的正极电极方程式:
。
(2)若Ag+导电,α-AgI本身质量将 。(填“不变”、“变大”、或“变小”,下同。)
若I-导电,阳极附近的α-AgI晶体密度将会 。
(3)若通电一段时间后铅蓄电池中消耗了1molH2SO4,则电解池的阴极增重 __________g。
23.工业上处理含Cr2O72-的酸性工业废水用以下方法:①往工业废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀生成,③过滤回收沉淀,废水达排放标准,试回答:
(1)电解时的电极反应,阳极_______________________,阴极____________________。
(2)写出Cr2O72-转变成Cr3+的离子反应______________________________________。
(3)电解过程中Cr(OH)3和Fe(OH)3沉淀是怎样产生的?
______________________________________________________________________。
(4)能否将Fe电极改成石墨电极?为什么?
________________________________________________________________________ 。
22.已知电极材料:铁、铜、银、石墨、锌、铝,电解质溶液:氯化铜溶液、硫酸铁溶液、盐酸。按要求回答下列问题:
①电工操作上规定:不能把铜导线和铝导线连接在一起使用,请说明原因。__________ 。
②若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? ,若能,请写出电极反应式,负极 ,正极 。(若不能后面两空不填)
③若电池反应为:Cu+2H+= Cu2++H2,该电池属于原电池还是电解池?请写出电极材料和电解质溶液。 _________________________________ 。
④有M、N两种金属分别与稀盐酸反应,产生氢气速率相近,请设计一个实验证明M、N两种金属的活泼性。 。
21. 在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插有两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体
,装置如图所示。接通电源,阳极周围的液体呈棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。回答:
在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插有两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体
,装置如图所示。接通电源,阳极周围的液体呈棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。回答:
(1)阳极上的电极反应式为 ;
阴极上的电极反应式为 。
(2)原上层液体是 ,原下层液体是 。
(3)搅拌后两层液体颜色发生变化的原因是
。
(4)要检验上层液体中含有的金属离子,其方法是 ;
现象是 。
20.电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
 (1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
① 电解池中X极上的电极反应式为 ,
在X极附近观察到的现象是 。
② Y电极上的电极反应式为 , 检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
① X电极的材料是 ,电极反应式是 。
② Y电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
19.火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为 。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
18.某混合溶液中只含有两种溶质NaCl和H2SO4,且n(NaCl)︰n(H2SO4)=3︰1。若以石墨电极电解该溶液,下列推断中不正确的是
A、阴极产物为H2 B、阳极先析出Cl2,后析出O2
C、电解液的pH不断增大,最终大于7 D、整个电解的过程实质是电解水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com