
题目列表(包括答案和解析)
28.(本题12 分)下图中的每一方格表示有关的一种反应物或生成物,其中A和C 为无色气体。
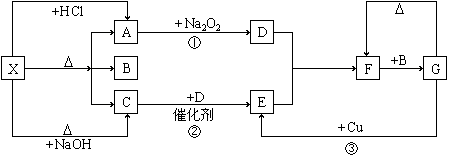
填写下列空白:
(1)物质X的化学式可以是 或 。
(2)C的分子式为 ,空间构型为 ,其分子是由 键形成的 分子,表示C的水溶液呈酸性或碱性的方程式为 。
(3)反应②的化学方程式为 ;
(4)G生成F的化学方程式为
27、(15分)某课外活动小组在实验室用下图的一些装置组合后,快速制取氨并验证氨的某些性质,同时收集少量纯净氮气,请回答:
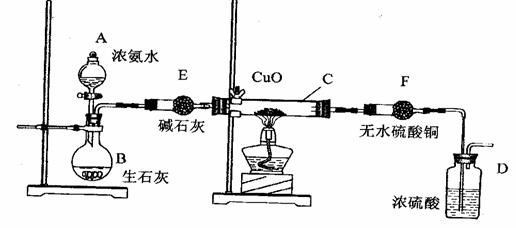
(1)写出烧瓶B中发生反应制氨气的化学方程式:
用平衡移动原理解释能用此法制取氨气的原因:
(2) 本实验进行一段时间后,观察到加热的硬质玻璃试管内黑色氧化铜粉末转为红色,盛无色硫酸铜的干燥管内出现蓝色,并且在最后的出气导管处收集到纯净、干燥的氮气。根据这些现象,写出在硬质玻璃试管内发生反应的化学方程式:_______________ __,这个反应说明氨气具有______________(填编号:A、碱性 ;B、还原性;C、氧化性; D、不稳定性)
(3) 洗气瓶D中盛浓硫酸的主要作用是 ________ _________。
(4) 在最后的出气的导管口收集干燥、纯净的氮气,收集方法是:___________
(填编号:A、排气法 B、排水法 C、用气囊收集)
(5)装置F的作用是____ _______________。
26.(4分)NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:(未配平)
 NaNO2
+ HI NO + I2 + NaI + H2O (1)若有1 mol的还原剂被氧化,则参加反应的氧化剂物质的量是 mol
NaNO2
+ HI NO + I2 + NaI + H2O (1)若有1 mol的还原剂被氧化,则参加反应的氧化剂物质的量是 mol
(2)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:① 水 ② 碘化钾淀粉试纸 ③ 淀粉 ④ 白酒 ⑤ 食醋,进行实验,下列几组合适的是 (填选项)。
A.③ ⑤ B.① ② ④ C.① ② ⑤
25、恒温、恒压下,1 A和
A和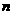
 B在一个容积可变的容器中发生如下反应:A(g)+2B(g)⇌ 2C(g) ,一段时间后达到平衡,生成
B在一个容积可变的容器中发生如下反应:A(g)+2B(g)⇌ 2C(g) ,一段时间后达到平衡,生成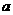
 C。则下列说法中正确的是( )
C。则下列说法中正确的是( )
A.物质A、B的转化率之比为1:2
B.起始时刻和达平衡后容器中的压强比为 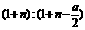
C.若起始时放入3 A和
A和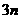
 B,,则达平衡时生成3
B,,则达平衡时生成3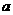
 C
C
D.当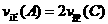 时,可断定反应达到平衡
时,可断定反应达到平衡
第Ⅱ卷 非选择题(共58分)
(本卷包括6个小题)
24、某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
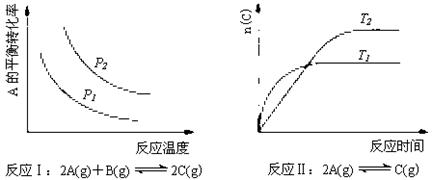
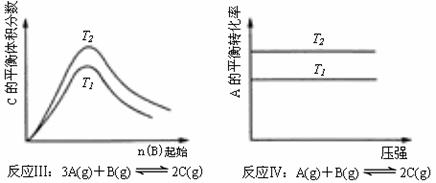
根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:△H>0,P2>P1
B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅲ:△H>0,T2<T1
D.反应Ⅳ:△H<0,T2>T1
23、氮气和氢气的混合气体对氦气的相对密度为1.8,取0.5mol该混合气体,在固定体积的容器中进行反应,当平衡时的压强是反应前压强的0.8倍时,平衡时,混合气体的总的物质的量为( )
A 0.1mol B 0.4mol C 0.6mol D 0.5mol
22、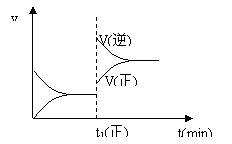 下图为某化学反应的速率与时间的关系示意图。在t1 时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
下图为某化学反应的速率与时间的关系示意图。在t1 时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
A.2SO2(g)+O2(g) ⇌ 2SO3(g) ; ΔH<0
B.4NH3(g)+5O2(g) ⇌ 4NO(g)+6H2O(g) ; ΔH<0
C.H2(g)+I2(g) ⇌ 2HI(g) ; ΔH>0
D.C(s)+H2O(g) ⇌ CO(g)+H2(g); ΔH>0
21、 往一个体积不变的密闭容器中充入H2和I2发生反应H2(g)+I2(g)≒2HI(g);△H>0,当达到平衡后,t0时改变某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是( )
往一个体积不变的密闭容器中充入H2和I2发生反应H2(g)+I2(g)≒2HI(g);△H>0,当达到平衡后,t0时改变某一条件(混合气体物质的量不变),且造成容器内压强增大,下列说法正确的是( )
A.容器内气体颜色不变,平均相对分子质量变小
B.平衡不移动,混合气体密度增大
C.H2的转化率增大,HI平衡浓度变小 D.改变条件前后,速率图象如上图
20、将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是 ( )
A. 反应速率:两者相同 B. 消耗硝酸的物质的量:前者多,后者少
C. 反应生成气体的颜色:前者浅,后者深
D. 反应中转移的电子总数:前者多,后者少
19.升高温度时,化学反应速率加快,主要原因是 ( )
A.分子运动速率加快,使该反应物分子的碰撞机会增多
B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多
C.该化学反应的过程是吸热的 D.该化学反应的过程是放热的
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com