
题目列表(包括答案和解析)
9、在室温下,0.1mol/L 100ml的醋酸溶液中,欲使其溶液的pH减小,但又要使醋酸电离程度减少,应采取( )
A 加入少量CH3COONa固体 B 通入少量氯化氢气体
C 提高温度 D 加入少量纯醋酸
8.下列操作中,能使电离平衡H2O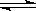 H++OH-向右移动且溶液呈酸性的是( )
H++OH-向右移动且溶液呈酸性的是( )
(A)向水中加入NaHSO4溶液 (B)向水中加入Al2(SO4)3溶液
(C)向水中加入Na2CO3溶液 (D)将水加热到100℃,使pH=6
7.室温下,在PH=12的碱溶液中,由水电离的c(H+)为( )
A. 1.0×10-12 mol·L-1 B.1.0×10-6 mol·L-1
C.1.0×10-2 mol·L-1 D. 1.0×10-7 mol·L-1
6.体积相同、溶质物质的量浓度也相同的HCl溶液和CH3COOH溶液,分别与NaOH溶液完全中和时,两者消耗NaOH的物质的量( )
A.相同 B.HCl多
C.CH3COOH多 D.无法比较
5.将8mol H2和2molN2充入2L密闭容器中,在一定条件下进行合成氨反应,4min后反应达到平衡,测得容器中还有5.6molH2。下列计算结果错误的是( )
(A)v(H2)=0.3 mol·L-1·min-1 (B)H2的转化率为25%
(C)NH3的物质的量浓度为0.8mol·L-1 (D)NH3的体积分数为19.05%
4、鉴别NO2气体和Br2蒸气,可用( )
A.湿润的淀粉KI试纸 B.AgNO3溶液 C.NaOH溶液 D.NaI溶液
3、下列各组离子在酸性溶液中由于发生氧化还原反应而不能大量共存的是( )
A.Na+、S2-、SO42-、SO32- B.Mg2+、Na+、Cl-、NO3-
C.Cl-、SO42-、Na+、Mg2+ D.K+、HCO3-、S2-、Na+
2、光化学烟雾是一次污染物(如氮氧化物、碳氢化合物等)发生光化学反应后生成的二次污染物,主要含有臭氧、过氧乙酰硝酸酯(CH3-COONO2)等。有关光化学烟雾的说法中不正确的是( )
A.光化学烟雾具有强氧化性
B.汽车尾气是造成光化学烟雾的最主要的原因
C.光化学烟雾对人体没有危害
D.光化学烟雾一般出现在强日照和低湿度、气温较高的条件下
1. 下列关于氮族元素的叙述不正确的是( )
A. 氮族元素都属于ⅤA族元素
B.通常都能和氢气直接化合生成稳定的氢化物
C. 单质的氧化性随核电荷数的增加逐渐减弱
D.随着原子序数递增,元素最高价氧化物的水化物的酸性减弱,碱性增强
23(14分)草酸晶体的组成可表示为:H2C2O4·XH2O,为测定X值,进行下列实验:
①称取wg草酸晶体配成100.0mL水溶液;
②取25.0mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为cmol/LKMnO4
滴定时,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
请回答下列问题:
(1)实验①中为配制准确浓度的草酸溶液,所需用到的仪器是:
天平(含砝码)、烧杯、药匙和 _________
(2)实验②中,滴定时,KMnO4溶液应装在 (填“酸式滴定管或碱式滴定管)
(3) 滴定中,目光应注视 _____________________ _
判断滴定结束的标准是 ___________________
(4)若滴定时,反应前后的两次读数分别为a和b,则实验测得所配草酸溶液的物质的量浓度为 ,由此计算出草酸晶体的X值是
____________________________________________________ _
(5)若在滴定前滴定管尖嘴部分留有气泡,滴定后滴定管尖嘴部分气泡消失,则测定的草酸溶液的物质的量浓度_____(偏大或偏小)
24(13分)某同学利用如图所示的装置进行中和热测定的实验,实验步骤如下:
①在大烧杯底部垫碎泡沫塑料,放入小烧杯,
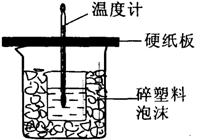 再在大、小烧杯之间填上碎纸条,
再在大、小烧杯之间填上碎纸条,
大烧杯上用硬纸板作盖板
②用一个量筒取50mL2.0 mol·L-1盐酸,
倒入小烧杯中,并用温度计测量盐酸的温度,
然后把温度计上的酸用水冲洗干净
③用另一个量筒取50mL2.0 mol·L-1NaOH溶液,
并用温度计测量NaOH溶液的温度
④把套有盖板的温度计放入小烧杯的盐酸中,并将量筒中的NaOH溶液缓缓倒入小烧
杯中(注意不要洒在外面),盖好盖板。用温度计轻轻搅动溶液(注意不要碰到烧杯底部或烧杯壁),并准确读取混合溶液的最高温度,记为终止温度
⑤________________________________________________________________________
⑥根据实验数据计算中和热
回答下列问题:
(1)请将上面第⑤步的实验步骤补充完整
(2)从实验装置上看,图中尚缺少的一种玻璃仪器是(量筒除外)__________________
(3)为保证该实验成功采取了许多措施,其中最主要的作用在于____________________
(4)在以上①--④步操作或装置图中,有许多不当之处,请一一指出(可不填满,也可补充)
I ______________________________________________________________________
II______________________________________________________________________
III_____________________________________________________________________
IV______________________________________________________________________
V______________________________________________________________________
VI_____________________________________________________________________
(5) 用正确的方法测得含有11.2克KOH的稀溶液与1L0.1 mol·L-1的H2SO4溶液反应,
放出11.46KJ热量,该反应的中和热化学方程式是
_______________________________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com