
题目列表(包括答案和解析)
23、(8分)
(1) A、B两化合物的分子式是 C5H9O4N 。
(2) 则A的结构简式为 谷氨酸 。
(3) 则B的结构简式是 OHC-(CH2)4-NO2 。
22、 (8分)(1)A.丙氨酸B.丙酸铵
(8分)(1)A.丙氨酸B.丙酸铵
(2)A+NaOH:
B+NaOH:CH3CH2COONH4+NaOH CH3CH2COONa+NH3↑+H2O
CH3CH2COONa+NH3↑+H2O
21、(4分)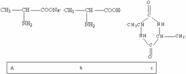
20、(8分)
(1)氯化铝是共价化合物 (2)化学式为 Al2Cl6 。
(3)无水氯化铝在空气中强烈的发“烟”,其原因是 发生水解
(4)设计一个可靠的实验,判断氯化铝是离子化合物还是共价化合物 熔融时是否导电 三、推断题(共3题,共20分)
19、(6分)
(1)X是 S ,Y是 O ,Z是 Na 。
(2)Z的单质属于 金属 晶体,Z与Y形成Z2Y的过程可用电子式表示为 略 。
18、(4分)(1)淡黄色溶解度小的是 黄绿色固体溶解度大的是

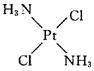
(2)因为分子结构不对称,所以分子有极性,因而在水中溶解度大。
17、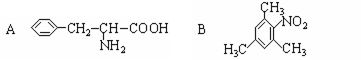 (4分)
(4分)
25、(6分)石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
①CH2=CH2+Cl2→CH2Cl-CH2Cl ②CH2Cl-CH2Cl→CH2=CHCl+HCl
请回答以下问题:
(1)已知反应①中二氯乙烷的产率(产率=实际产量/理论产量´100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯 t,同时得到副产物氯化氢 t(计算结果保留1位小数);
(2)为充分利用副产物氯化氢,该工厂后来将下列反应运用于生产:
③2CH2=CH2+4HCl+O2→2CH2Cl-CH2Cl+2H2O
由反应①、③获得二氯乙烷,再将二氯乙烷通过反应②得到氯乙烯和副产物氯化氢,副产物氯化氢供反应③使用,形成了新的工艺。
由于副反应的存在,生产中投入的乙烯全部被消耗时,反应①、③中二氯乙烷的产率依次为a%、c%;二氯乙烷全部被消耗时,反应②中氯化氢的产率为b%。试计算:反应①、③中乙烯的投料比为多少时,新工艺既不需要购进氯化氢为原料,又没有副产物氯化氢剩余(假设在发生的副反应中既不生成氯化氢,也不消耗氯化氢)。
高二化学试题
卷Ⅰ(选择题,共48分)
卷Ⅱ(非选择题,共52分)
23、(4分)1986年,瑞士两位科学家发现一种性能良好的金属氧化物超导体,使超导工作取得突破性进展,为此两位科学家获得了1987年的Nobel物理学奖。其晶胞结构如图。
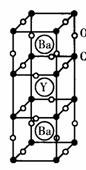 (1)根据图示晶胞结构,推算晶体中Y,Cu,Ba和O原子个数比为 。
(1)根据图示晶胞结构,推算晶体中Y,Cu,Ba和O原子个数比为 。
(2)该化合物中各元素的化合价为Y为+3价,Ba为+2价,Cu为+2和+3价,根据化合物的组成,计算化合物中+2价Cu与+3价Cu原子个数比为 。
22、(8分)有机物A的分子式为C3H7O2N,有机物B的分子式为C3H9O2N,这两种有机物的分子结构中都有一个与碳原子相连的甲基,它们都能与NaOH溶液反应,也都能与H2SO4反应,请填写以下空格:
(1)有机物A、B的结构简式:A ,B 。
(2)A与盐酸反应的化学方程式: ;
B与NaOH反应的化学方程式: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com