
题目列表(包括答案和解析)
2、下列说法正确的是:( )
A、增大反应物浓度,能增大活化分子百分数,所以反应速率增大
B、使用催化剂,能增大活化分子数,所以反应速率增大
C、对于任何反应,增大压强都可以加快反应速率
D、升高温度,只能增大吸热反应的反应速率
1、下列有关化学反应速率的说法正确的是:( )
A、用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B、2mol/ L100ml的盐酸和锌片反应,加入适量的氯化钠溶液,反应速率不变
C、SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢
D、汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢
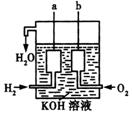
23. (11分)美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
(1)a是__________极;b是____________极。电极反应式分别为_____________________、________________________________;
|
已知: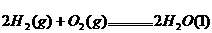 ;
;
(3)当这种电池使小灯泡连续发光一段时间后,耗电能为5.4KJ,则消耗标准状况下的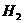 多少升?
多少升?
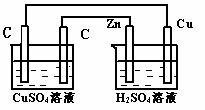
22.(10分)现有一个装有某种电解质溶液的烧杯,某一电池,两根石墨电极,一根锌电极,一根铁电极,一根铜电极和导线,你能选用上述仪器和药品设计一个简单实验来判断某电池的正负极吗?(电解质溶液任选)
 (1)请你画出进行该实验的装置图:
(1)请你画出进行该实验的装置图:
(2)实验现象及结论是:
。
(3)电极反应方程式:__________________________________
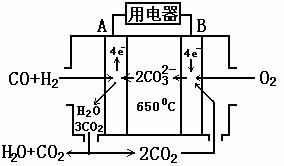
21.(8分)熔融碳酸盐燃料电池(MCFS),发明于1889年,上世纪的30-60年代在荷兰得到广泛的发展,而且建成了寿命超过40000小时的电池,可应用于中心电站。现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质。操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2)直接作燃料,其工作原理如图所示。请回答下列问题:
(1)B极为 极,发生 (填“氧化”或“还原”)反应,该极发生的电极反应为 ;
(2)电池总反应为_________________________ 。
20. (10分)已知电极材料:铁、铜、银、石墨、锌、铝,电解质溶液:氯化铜溶液、硫酸铁溶液、盐酸。按要求回答下列问题:(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用,请说明原因。
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? ,若能,请写出电极反应式,负极 ,正极 。若不能后面两空不填。
 (3)若电池反应为:Cu+2H+= Cu2++H2,该电池属于原电池还是电解池?请写出电极材料和电解质溶液。
(3)若电池反应为:Cu+2H+= Cu2++H2,该电池属于原电池还是电解池?请写出电极材料和电解质溶液。
19.(8分)以A、B两根石墨棒作电极,电解硝酸银溶液,通电10分钟时,在B极收集到气体11.2毫升(标况);然后将电源反接,以相同的电流强度再通电5分钟,此时与第一次通电前相比较,两极的质量变化分别是A极__________、 B极________(填增大、减少、不变) ,其数值分别是A_________ 、 B________ ;
若溶液的体积为200毫升(设体积不变),则溶液的pH值为__________。
18.(9分)据报道,最近摩托罗拉(MOTOROLA)公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用1个月充电一次。假定放电过程中,甲醇完全氧化产生的CO2被充分吸收生成CO32-
(1)该电池反应的总离子方程式为_______________________。
(2)甲醇在____极发生反应(填正或负),电池在放电过程中溶液的pH将____(填降低或上升、不变);若有16克甲醇蒸气被完全氧化,则转移的电子物质的量为________。
(3)最近,又有科学家制造出一种固体电解质的燃料电池,其效率更高。一个电极通入空气,另一电极通入汽油蒸气。其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2(Zr:锆)固体,它在高温下能传导O2-离子(其中氧化反应发生完全)。以丁烷(C4H10)代表汽油。
①电池的正极反应式为_________________________________________。
②放电时固体电解质里的O2-离子的移动方向是向_____极移动(填正或负)。
17.(8分)锌-锰干电池是普遍使用的化学电池,其中含有MnO2、NH4Cl、ZnCl2等糊状物。以锌筒为负极材料,石墨为正极材料。工作时反应方程式是:
Zn+2MnO2+2NH4+=Zn2++Mn2O3+2NH3+H2O
(1)试写出干电池放电时的正、负电极反应式:
正极:_________________________负极:______________________
干电池用久了就会变软,其原因是____________________________。
(2)正极反应中,前后经历下列反应:2NH4++2e-=2NH3+H2;2MnO2+H2=Mn2O3+H2O,如果没有MnO2参与,干电池将难于持续稳定工作。
试说明理由:_______________________________________________。
15. 柯尔贝反应是:2RCOOK+2H2O--→ R-R+2CO2+H2+2KOH(式中“R-”代表烃基)。下列说法正确的是 ( )
A.含碳元素的产物均在阴极区生成
B.含碳元素的产物均在阳极区生成
C.含氢元素的产物均在阳极区生成
 D.CO2在阴极逸出,H2在阳极逸出
D.CO2在阴极逸出,H2在阳极逸出
|
|
A.相同条件下,两容器中产生气体体积相同
B.①、②溶液的pH均减小
C.①中阳极电极反应式为:4OH一一4e一= 2H2O+O2↑
D.①中阴极上析出0.64g铜
第Ⅱ卷 (非选择题 共64分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com