

题目列表(包括答案和解析)
4分。共68分。每小题只有一个选项符合题意。)
1.纤维素被称为“第七营养素”,食物中的纤维素虽然不能为人体提供能量,但能促进肠道蠕动和分泌消化液,有助于食物的消化和废物的排泄,从化学成分看,它是一种
A.二糖 B.多糖 C.氨基酸 D.脂肪
25.(10分)镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:
Cd+2NiO(OH)+2H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
(1)若用此电池作电源电解足量的M(NO3)x溶液(用碳棒作电极材料),电解池的阳极
应连接 (填序号) ①NiO(OH) ②Cd ③Cd(OH)2 ④Ni(OH)2
电池的负极反应为
当该电池工作一段时间后消耗了3.6gH2O时,电解池某极增重m g,则金属M的相对
原子质量为 (用m、x表示)。
(2)若用此电池作电源电解含有0.1molCuSO4和0.1molNaCl的混合溶液100mL(用碳棒作电极材料),
当电路中有0.2mole-通过时,阳极产生气体多少升(标准状况)?
电解后溶液加水稀释至1L,常温下溶液的pH是多少?

24.(10分)已知:CH3CH2OH+NaBr+H2SO4(浓) CH3CH2Br+NaHSO4
+H2O。
CH3CH2Br+NaHSO4
+H2O。
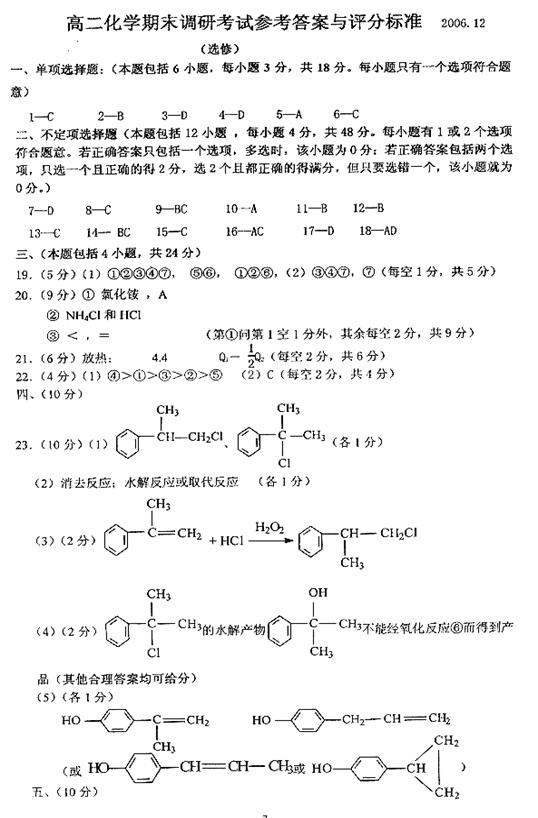
 实验室制备溴乙烷(C2H5Br)的装置和步骤如下:
实验室制备溴乙烷(C2H5Br)的装置和步骤如下:
(已知溴乙烷的沸点为38.4℃):
①按右图所示连接仪器装配装置,检查装置的气密性,然后向装置中的
U形管和大烧杯里加入冰水;
②在圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的
13g溴化钠和几粒碎瓷片
③小火加热,使其充分反应,
回答下列问题:
(1)反应时若温度过高可看到有红棕色气体产生,该气体化学式为
(2)反应结束后,U形管中粗制的溴乙烷呈棕黄色。将U形管中的混合物倒入分液漏斗中,静置,
待液体分层后,取 (填“上层”或“下层”) 液体。
为了除去其中的杂质,最好选择下列试剂中的 (填序号)。
a.Na2SO3溶液 b.H2O c.NaOH浓溶液 d.CCl4
要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行
(填操作名称)。
(3)下列几项实验步骤,可用于检验溴乙烷中的溴元素,其正确的操作顺序是:
取少量溴乙烷,然后 (填代号)。
①加热; ②加入AgNO3溶液; ③加入稀HNO3酸化; ④加入NaOH溶液; ⑤冷却。
请写出在此过程中,有溴乙烷参加的反应的化学方程式 ,
检验此反应中有机产物可用 的方法。
2.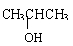 在铜或银作催化剂的条件下,被空气中氧气氧化不能生成CH3CH2CHO。
在铜或银作催化剂的条件下,被空气中氧气氧化不能生成CH3CH2CHO。
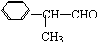 工业上利用上述信息,按下列路线合成结构简式为 的物质,该物质是一种香料。
工业上利用上述信息,按下列路线合成结构简式为 的物质,该物质是一种香料。
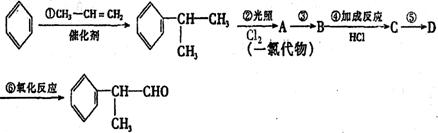
请根据上述路线,回答下列问题:
(1) A中的一氯代物有两种,它们的结构简式为 和
(2) ③、⑤的反应类型分别为 、
(3) 反应④的化学方程式为(有机物写结构简式,并注明反应条件):
(4) 工业生产中,中间产物A须经反应③④⑤得D,而不采取直接转化为D的方法,
其原因是 。
(5) 这种香料具有多种同分异构体,其中某些物质有下列特征:
①含有酚羟基 ②分子中有苯环,且苯环上的一溴代物有两种。
写出符合上述条件的物质可能的结构简式(只写两种): , 。
23.(10分)已知:1.有机化学反应因反应条件不同,可生成不同的有机产品。

(2)苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;
若在催化剂作用下,苯环上的氢原子被卤素原子取代。
22.(4分)(1)对于难溶盐MX,其饱和溶液中M+和X-的物质的量浓度之间的关系类
似于c(H+)·c(OH-)=Kw,存在等式c(M+)·c(X-)=Ksp。现将足量的AgCl分别放
入下列物质中,AgCl的溶解度由大到小的排列顺序是 (填序号)
①20mL0.01mol/LKCl溶液 ②30mL0.02mol/LCaCl2溶液
③40mL0.03mol/LHCl溶液 ④10mL蒸馏水⑤50mL0.05mol/LAgNO3溶液
(2)向5mL NaCl溶液中滴人一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振
荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变为黑色,根据上述变化过程,
分析此三种沉淀物的溶解度关系为
A.AgCl=AgI=Ag2S B.AgCl<AgI<Ag2S
C.AgCl>AgI>Ag2S D.AgI>AgCl>Ag2S
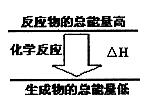
21.(6分)(1)化学反应中均伴随着能量的变化。如果一个化学反应中,
反应物的总能量和生成物的总能量有如图所示的关系,则该反应
过程中的能量变化是 (填“放热”或“吸热”)
已知热化学方程式为:
C(s)+O2(g)===CO2(g) ; △H=-393.5 kJ/mol
H2(g)+1/2O2(g)===H2O(l) ; △H=-285.8kJ/mol
试通过计算说明等质量的氢气和碳燃烧时产生热量的比值是 (保留1位小数)。
(2) 已知Mg(s)+1/2O2(g)=MgO(s);△H=Q1 , 2Hg(l)+O2(g)=2HgO(s) ;△H=Q2
现有反应Mg(s)+HgO(s)=Hg(L)+MgO(s) ;△H=Q3。则Q3应为
(用含Q1、Q2的式子表示)
20.( 9分)已知某溶液中只存在OH-、H+、NH4+、Cl四种离子,某同学推测该溶液中各离子
浓度大小顺序可能有如下四种关系:
A.c(C1-)>c(NH4十)>c(H+)>c(OH-) B.c(C1-)>c(NH4+)>c(OH-)>c(H+)
C.c(C1-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,这种溶质的名称是 ,该溶液中离子浓度大小顺序
关系是(选填序号)
②若上述关系中C是正确的,则溶液中溶质的化学式是
③若该溶液由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前
c(HCl) c(NH3·H2O) (填“>”、“<”、或“=”,下同)混合后溶液中c(NH4+)与
 c(Cl-)的关系是c(NH4+) c(Cl-)。
c(Cl-)的关系是c(NH4+) c(Cl-)。
19.
 (5分)按要求对下列化合物进行分类:
(5分)按要求对下列化合物进行分类:
①CH3CH2CH3 ②CH2=CH2 ③CH3CH2OH ④CH3CH2Br ⑤ ⑥
⑦CH3COOCH2CH3
(1)按碳的骨架分类,属于链状化合物的是(填写编号,下同) 。属于环状化合物的
是 属于脂肪烃的是 。
(2)按照组成元素、官能团和结构特点分类,属于烃的衍生物的是
其中属于酯的是
18.在一个固定体积的密闭容器中,保持一定温度,进行以下反应:
H2(g)+Br2(g) 2HBr(g), 已知加入lmol H2和2mol Br2时,反应达到平衡后,生成amol
2HBr(g), 已知加入lmol H2和2mol Br2时,反应达到平衡后,生成amol
HBr。在相同条件下,起始时加入H2、Br2、HBr的物质的量分别为x、y、z(均不为零),
如果仍保持平衡后各组分的物质的量分数不变,以下推断不正确的是
A.x、y、z应满足的关系是y=2x+z B.x、y、z应满足的关系是4x十z=2y
C.达到平衡时HBr物质的量为(x+y+z)a/3 D.达到平衡时HBr物质的量一定仍为amol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com