
题目列表(包括答案和解析)
15. 从下列现象可以判断某酸是强酸的是
A.加热该酸至沸腾也不分解 B.该酸可以分解石灰石放出CO2
C.该酸可以把Al(OH)3沉淀溶解 D.该酸浓度为0.1mol·L-1时的pH为1
14.取pH值均等于2的盐酸和醋酸各100mL分别稀释二倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
A. 醋酸与锌反应放出氢气多 B. 盐酸和醋酸分别与锌反应放出的氢气一样多
C. 醋酸与锌反应速率小 D. 盐酸和醋酸分别与锌反应的速度一样大
13.某强酸溶液pH=a , 强碱溶液pH=b, 已知a+b=16,在常温下混合后pH=7,则酸溶液体积V酸和碱溶液的体积V碱的准确关系是:
A. V碱=102V酸 B. V酸=102V碱 C. V酸=2V碱 D. V碱=2V酸
12.用水稀释0.1mol/L的醋酸溶液,其中随水的增加而最终增大的有
①H+的物质的量 ②c(H+) ③c(OH-) ④c(H+)/c(HAc) ⑤c(HAc)/c(Ac-)
A. ①③④ B. ①③⑤ C. ②④ D. ③④
11.将pH=8的Ba(OH)2溶液加水稀释1000倍,稀释后所得溶液中Ba2+浓度与OH-浓度之比为
A. 1:2 B. 1:200 C.1:50 D. 1:100
10.pH=9的Ba(OH)2溶液与pH=12的KOH溶液,按4:1的体积比混合,则溶液中c(H+)为(mol/L)
A. (4×10-9 + 1×10-12) 1/5 B. (8×10-9 + 1×10-12) 1/5 C. 5×10-10 D. 5×10-12
9.对于平衡体系:mA(g)+nB(g) pC(g)+qD(g);△H<0. 有下列判断,其中正确的是
pC(g)+qD(g);△H<0. 有下列判断,其中正确的是
A.若温度不变,将容器的容积增大1倍,此时A的浓度变为原来的0.45倍,则m+n>p+q
B.若平衡时,A.B的转化率相等,说明反应开始时,A.B的物质的量之比为m∶n
C.若平衡体系共有气体amol,再向其中加入bmolB,当重新达到平衡时,气体的总物质的量等于a+b,则(m+n)>(p+q)
D.温度不变时,若压强增大2倍,达到新平衡时,总体积一定比原体积的1/2要小
8.在2L密闭容器中加入或通入一定量A、B、C三种物质,在一定条件下发生反应(如图1),3min后给体系加热,气体C的体积分数Ψ(C)和混合气体的平均相对分子质量M均随温度分别发生了图示变化(如图2、图3)。下列有关说法不正确的是
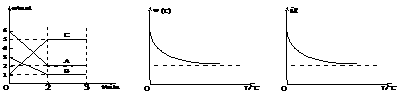
图1 图2 图3
A.前2min中C的平均反应速率为1mol/L·min B.该反应的化学方程式为:2A+B 2C
2C
C.正反应是放热反应 D.A、B一定均为气态
7.恒温恒压下,在容积可变的密闭容器中发生如下反应:A(g)+ B(g) C(g)。若开始时通入1molA和1molB,到达平衡后生成amolC,则下列说法错误的是
C(g)。若开始时通入1molA和1molB,到达平衡后生成amolC,则下列说法错误的是
A.若开始时通入3molA和3molB,到达平衡后,生成C的物质的量为3amol
B.若开始时通入xmolA、2molB和1molC,到达平衡后,A和C的物质的量分别为ymol和3amol,则x = 2,y = 3-3a
C.若开始时通入4molA、2molB和1molC,到达平衡后,B的物质的量一定大于2mol
D.若开始时通入2molA、2molB和1molC,到达平衡后,再通入3molC,则再次达平衡后,C的物质的量分数为a / (2-a)
6.如右图,向A中充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于aL,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应:X(g)+
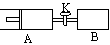 Y(g)
Y(g) 2Z(g) + W(g);△H<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g) + W(g);△H<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是
A.反应速率:v(B)> v(A) B.A容器中X的转化率为80%
C.平衡时的压强:PB = 2PA D.平衡时Y的体积分数:A<B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com