
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
1.ЯТСаЮяжЪЕФЫЎШмвКФмЕМЕчЃЌЕЋЪєгкЗЧЕчНтжЪЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
A.HClOЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.Cl2ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.NH4HCO3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.SO2
34.25ЁцЪБЃЌШєpH=aЕФ10ЬхЛ§ЕФФГЧПЫсШмвКгыpH=b ЕФ1ЬхЛ§ЕФФГЧПМюШмвКЛьКЯКѓШмвКГЪжаадЃЌдђЛьКЯжЎЧАИУЧПЫсЕФpHгыЧПМюЕФpHжЎМфгІТњзуЕФЙиЯЕЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
33.ЯжгаS2ЃЁЂSO32ЃЁЂNH4+ЁЂAl3+ЁЂHPO42ЃЁЂNa+ЁЂSO42ЃЁЂAlO2ЃЁЂFe3+ЁЂ
HCO3ЃЁЂClЃЕШРызгЃЌЧыАДвЊЧѓЬюПеЃК
ЂХдкЫЎШмвКжаЃЌИУРызгЫЎНтГЪМюадЕФЪЧЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЦдкЫЎШмвКжаЃЌИУРызгЫЎНтГЪЫсадЕФЪЧЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЧМШФмдкЫсадНЯЧПЕФШмвКРяДѓСПДцдкЃЌгжФмдкМюадНЯЧПЕФШмвКРяДѓСПДцдкЕФРызггаЃКЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂШМШВЛФмдкЫсадНЯЧПЕФШмвКРяДѓСПДцдкЃЌгжВЛФмдкМюадНЯЧПЕФШмвКРяДѓСПДцдкЕФРызггаЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
32ЃЎгвЭМЮЊжмЦкБэЕФвЛаЁВПЗжЃЌAЁЂBЁЂCЁЂDЁЂEЕФЮЛжУЙиЯЕШчЭМ
ЫљЪОЁЃЦфжаBдЊЫиЕФзюИпМлЪЧИКМлОјЖджЕЕФ3БЖЃЌЫќЕФзюИпбѕЛЏЮяжа
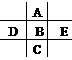
КЌбѕ60%ЃЌЛиД№ЯТСаЮЪЬтЃК
(1)AЕФжЪСПЪ§ЪЧ____ЃЌЮЛгкЕк_____жмЦкЃЌЕк_____зхЁЃ
(2)ЗжБ№аДГівдЯТзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮя:
BЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЁЁЁЁЁЁЁЁЁЁЁЁ EЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
BЁЂCЁЂEШ§жждЊЫиЕФЦјЬЌЧтЛЏЮяЦфЮШЖЈадгЩЧПЕНШѕЦіЕФЫГађЪЧ
ЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
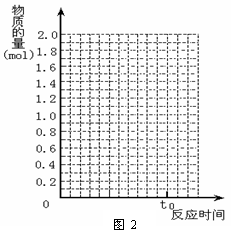
31.ШчЭМ1ЃЌНЋ2 mol SO2КЭ1 mol O2ЛьКЯжУгкЬхЛ§ПЩБфЕФУмБеШнЦїжаЃЌдкT1ЮТЖШЯТЗЂЩњШч
ЯТЗДгІЃК2SO2(g)+O2(g) 2SO3(g)ЃЛЁїHЃМ0ЁЃ
2SO3(g)ЃЛЁїHЃМ0ЁЃ
ЕБЗДгІНјааЕНЪБМфt0ЪБДяЕНЦНКтзДЬЌЃЌВтЕУЛьКЯЦјЬхЕФзмЮяжЪЕФСПЮЊ2.1 molЁЃЪдЛиД№ЃК
(1)дкЭМ2жазїГіЗДгІЛьКЯЮяжаИїзщЗжЦјЬхЕФЮяжЪЕФСПЫцЗДгІНјааЕНt0ЪБЕФБфЛЏЧњЯпЃЛ
 (2)ЕБЗДгІНјааЕНt1ЪБМфЪБ(t1ЃОt0)ЃЌИјЩЯЪіЗДгІШнЦїМгШШЕНЮТЖШЮЊT2 (T2ЃОT1)ЃЌЗДгІдкt3ЁЁЪБМфЪБ (t3ЃОt1)жиаТДяЕНЦНКтзДЁЁЬЌЃЌаТЦНКтЛьКЯЮяжаЦјЬхЕФзмЮяжЪЕФСПЁЁ________2.1 mol(ЬюЁАЃМЁБЁЂЁАЃОЁБЛђЁАЃНЁБ)ЁЃ
(2)ЕБЗДгІНјааЕНt1ЪБМфЪБ(t1ЃОt0)ЃЌИјЩЯЪіЗДгІШнЦїМгШШЕНЮТЖШЮЊT2 (T2ЃОT1)ЃЌЗДгІдкt3ЁЁЪБМфЪБ (t3ЃОt1)жиаТДяЕНЦНКтзДЁЁЬЌЃЌаТЦНКтЛьКЯЮяжаЦјЬхЕФзмЮяжЪЕФСПЁЁ________2.1 mol(ЬюЁАЃМЁБЁЂЁАЃОЁБЛђЁАЃНЁБ)ЁЃ
(3)ШєЦ№ЪМЪБМгШы0.6 mol SO2ЁЂ0.3 mol O2КЭx mol SO3ЃЌБЃГжЮТЖШ
ВЛБфЃЌДяЕНЦНКтзДЬЌКѓЃЌИїЦјЬхЕФЬхЛ§ЗжЪ§гыЩЯЪіЦНКтзДЬЌЯрЭЌЃЌx
ЕФжЕЮЊ__________ЁЃ
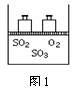
30.гаМзЁЂввСНИіШнЛ§ЯрЕШЕФКуШнУмБеШнЦїЃЌЯђМзжаЭЈШы6mol AКЭ2mol
BЃЌЯђввжаЭЈШы1.5mol AЁЂ0.5mol BКЭ3molCКЭ2molDЃЌНЋСНШнЦїЕФЮТЖШКуЖЈдк770KЃЌЪЙЗДгІ3A(g)+B(g) xC(g) +D(s)ДяЕНЦНКтЃЌДЫЪБВтЕУМзЁЂввСНШнЦїжаCЕФЬхЛ§ЗжЪ§ЖМЮЊ0.2ЃЌЪдЛиД№ЯТСагаЙиЮЪЬтЃК
xC(g) +D(s)ДяЕНЦНКтЃЌДЫЪБВтЕУМзЁЂввСНШнЦїжаCЕФЬхЛ§ЗжЪ§ЖМЮЊ0.2ЃЌЪдЛиД№ЯТСагаЙиЮЪЬтЃК
(1)ШєЦНКтЪБЃЌМзЁЂввСНШнЦїжаAЕФЮяжЪЕФСПЯрЕШЃЌдђx=_________ЃЛШєЦНКтЪБЃЌМзЁЂввСНШнЦїжаAЕФЮяжЪЕФСПВЛЯрЕШЃЌдђx=_________ЁЃ
(2)ЦНКтЪБМзЁЂввСНШнЦїжаAЁЂBЕФЮяжЪЕФСПжЎБШЪЧЗёЯрЕШ____________(ЬюЁАЯрЕШЁБЛђЁАВЛЯрЕШЁБ)ЃЌЦНКтЪБМзжаAЕФЬхЛ§ЗжЪ§ЮЊ____________ЁЃ
(3)ШєЦНКтЪБЃЌМзЁЂввСНШнЦїжаAЕФЮяжЪЕФСПЯрЕШЃЌИФЮЊАДВЛЭЌХфБШзїЮЊввЕФЦ№ЪМЮяжЪЃЌДяЕНЦНКтКѓЃЌCЕФЬхЛ§ЗжЪ§ЖМШдЮЊ0.2ЁЃ
ЂйЗДгІДгФцЗДгІЗНЯђПЊЪМЃЌдђDЕФЦ№ЪМЮяжЪЕФСПгІТњзуЕФЬѕМўЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкШєМгШы0.6molAКЭ0.2molBЃЌдђCКЭDЦ№ЪМЮяжЪЕФСПЗжБ№гІТњзуЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ,ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
 (4)ШєЦНКтЪБСНШнЦїжаЕФбЙЧПВЛЯрЕШЃЌдђСНШнЦїжабЙЧПжЎБШЮЊЁЁЁЁ ЁЁЃКЁЁЁЁ ЁЃ
(4)ШєЦНКтЪБСНШнЦїжаЕФбЙЧПВЛЯрЕШЃЌдђСНШнЦїжабЙЧПжЎБШЮЊЁЁЁЁ ЁЁЃКЁЁЁЁ ЁЃ
29.вбжЊПЩФцЗДгІCO (g)+ H2O(g) CO2
(g)+ H2(g)ЃЌДяЕНЦНКтЪБЃЌK =c (CO2)ЁСc (H2)/c (CO)ЁСc (H2O)ЃЌKЪЧГЃЪ§ЃЌжЛгыЮТЖШгаЙиЃЌгыХЈЖШЮоЙиЁЃ
CO2
(g)+ H2(g)ЃЌДяЕНЦНКтЪБЃЌK =c (CO2)ЁСc (H2)/c (CO)ЁСc (H2O)ЃЌKЪЧГЃЪ§ЃЌжЛгыЮТЖШгаЙиЃЌгыХЈЖШЮоЙиЁЃ
(1)830KЪБЃЌШєЦ№ЪМЪБЃКc (CO) = 2 mol/LЃЌc (H2O) = 3 mol/LЃЌЦНКтЪБCOЕФзЊЛЏТЪЮЊ60%ЃЌЫЎеєЦјЕФзЊЛЏТЪЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЃЛKжЕЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)830KЃЌШєжЛНЋЦ№ЪМЪБc (H2O)ИФЮЊ6 mol/LЃЌдђЫЎеєЦјЕФзЊЛЏТЪЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)Шє830KЪБЃЌЦ№ЪМХЈЖШc (CO) = a mol/LЃЌc (H2O) = b mol/LЃЌH2ЕФЦНКтХЈЖШc (H2) = c mol/LЃЌ
ЂйaЁЂbЁЂcжЎМфЕФЙиЯЕЪНЪЧ____________________ЁЁЁЁЁЁЁЁ _ЃЛЂкЕБa = bЪБЃЌa = ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁcЁЃ
28.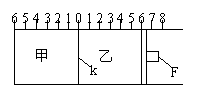 (I)ШчЭМЫљЪОЃЌМзЁЂввжЎМфЕФИєАхKКЭЛюШћFЖМПЩзѓгввЦЖЏЃЌМзжаГфШы2molAКЭ1molBЃЌввжаГфШы2molCКЭ1molHeЃЌДЫЪБKЭЃдк0ДІЁЃдквЛЖЈЬѕМўЯТЗЂЩњПЩФцЗДгІЃК2A(g)+B(g)
(I)ШчЭМЫљЪОЃЌМзЁЂввжЎМфЕФИєАхKКЭЛюШћFЖМПЩзѓгввЦЖЏЃЌМзжаГфШы2molAКЭ1molBЃЌввжаГфШы2molCКЭ1molHeЃЌДЫЪБKЭЃдк0ДІЁЃдквЛЖЈЬѕМўЯТЗЂЩњПЩФцЗДгІЃК2A(g)+B(g) 2C(g)ЃЛЗДгІДяЕНЦНКтКѓЃЌдйЛжИДжСдЮТЖШЁЃЛиД№ЯТСаЮЪЬтЃК
2C(g)ЃЛЗДгІДяЕНЦНКтКѓЃЌдйЛжИДжСдЮТЖШЁЃЛиД№ЯТСаЮЪЬтЃК
(1)ПЩИљОнЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЯжЯѓРДХаЖЯМзЁЂввЖМвбДяЕНЦНКтЁЃ
(2)ДяЕНЦНКтЪБЃЌИєАхKзюжеЭЃСєдк0ПЬЖШзѓВрaДІЃЌ дђaЕФШЁжЕ
ЗЖЮЇЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ШєДяЕНЦНКтЪБЃЌИєАхKзюжеЭЃСєдкзѓВрПЬЖШ1ДІЃЌдђМзжаCЕФЮя
жЪЕФСПЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁ molЃЌввжаCЕФзЊЛЏТЪЁЁЁЁЁЁЁЁ 50%(ЬюЃКЁАЃОЁБЁЂЁАЃМЁЂЁБЁАЃНЁБ)ЃЌДЫЪБЃЌввжаПЩвЦЖЏЛюШћFзюжеЭЃСєдкгвВрПЬЖШЁЁЁЁЁЁЁЁ ДІ(ЬюЯТСаађКХ)Ђй ЃМ6 ЁЁЁЁЁЁЂк ЃО6 ЁЁЁЁЁЁЂл ЃН6ЁЃ
(4)ШєДяЕНЦНКтЪБЃЌИєАхKзюжеЭЃСєдкзѓВрПЬЖШППНќ0ДІЃЌдђввжаПЩвЦЖЏЛюШћFзюжеЭЃСєдкгвВрЕФПЬЖШВЛДѓгкЁЁЁЁЁЁ ЃЛШєKзюжеЭЃСєдкзѓВрПЬЖШППНќ2ДІЃЌдђввжаFзюжеЭЃСєдкгвВрЕФПЬЖШВЛаЁгкЁЁЁЁЁЁ ЁЃ
(Ђђ)ШєвЛПЊЪМОЭНЋKЁЂFЙЬЖЈЃЌЦфЫќЬѕМўОљВЛБфЃЌдђДяЕНЦНКтЪБЃК
(1)МзЁЂввжаCЕФЮяжЪЕФСПЗжЪ§ЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЃКЁАМзЃОввЁБЛђЁАМзЃМввЁБЛђЁАМзЃНввЁБ )ЃЛ
(2)ВтЕУМзжаAЕФзЊЛЏТЪЮЊbЃЌдђввжаCЕФзЊЛЏТЪЮЊЁЁ ЁЁЁЁЁЁЃЛ
(3)МйЩшввЁЂМзСНШнЦїжаЕФбЙЧПБШгУdБэЪОЃЌдђdЕФШЁжЕЗЖЮЇЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
27.AЪЧгЩЕМШШВФСЯжЦГЩЕФУмБеШнЦїЃЌBЪЧвЛФЭЛЏбЇИЏЪДЧввзгкДЋШШЕФЦјЧђЁЃЙиБеK2ЃЌНЋЕШСПЧвЩйСПЕФNO2ЭЈЙ§K1ЁЂK3ЗжБ№ГфШЫAЁЂBжаЃЌЗДгІЦ№ЪМЪБЃЌAЁЂBЕФЬхЛ§ЯрЭЌЁЃ(вбжЊЃК2NO2 (g) N2O4(g)ЃЛЁїH<0)
N2O4(g)ЃЛЁїH<0)
(1)вЛЖЮЪБМфКѓЃЌЗДгІДяЕНЦНКтЃЌДЫЪБAЁЂBжаЩњГЩЕФN2O4ЕФЫйТЪЪЧVA_______VBЁЃ(ЬюЁАЃОЁБЁЂЁАЃМЁЂЁБЁАЃНЁБ)ЃЛШєДђПЊЛюШћK2ЃЌЦјЧђBНЋ__________(ЬюЃКЁАБфДѓЁБЁЂЁАБфаЁЁБЁЂЁАВЛБфЁБ)ЁЃ
(2)ШєдкAЁЂBжадйГфШЫгыГѕЪМСПЯрЕШЕФNO2ЃЌдђДяЕНЦНКтЪБЃЌNO2ЕФзЊЛЏТЪІСAНЋ_________ (ЬюЁАдіДѓЁБЛђЁАМѕаЁЁБЁЂЁАВЛБфЁБ)ЃЛШєЭЈШЫЕШСПЕФNeЦјЃЌдђДяЕНЦНКтЪБЃЌAжаNO2ЕФзЊЛЏТЪНЋ_________ЃЌBжаNO2ЕФзЊЛЏТЪНЋЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАБфДѓЁБЁЂЁАБфаЁЁБЛђЁАВЛБфЁБ)ЁЃ
(3)ЪвЮТЯТЃЌШєAЁЂBЖМБЃГжЬхЛ§ВЛБфЃЌНЋAЬзЩЯвЛИіОјШШВуЃЌBгыЭтНчПЩвдНјааШШДЋЕнЃЌдђДяЕНЦНКтЪБЃЌ_________жаЕФбеЩЋНЯЩюЁЃ
(4)ШєдкШнЦїAжаГфШЫ4.6gЕФNO2ЃЌДяЕНЦНКтКѓШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЮЊ57.5ЃЌдђЦНКтЪБN2O4ЕФЮяжЪЕФСПЮЊ_________ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
26.ЯТСаЫФжжШмвКжаЃЌгЩЫЎЕчРыЩњГЩЕФЧтРызгХЈЖШжЎБШ(ЂйЁУЂкЁУЂлЁУЂм)ЪЧЃКЂй1mol/LЕФбЮЫсЃЛЂк0.1 molЁЄLЃ1ЕФбЮЫсЃЛЂл0.01 molЁЄLЃ1ЕФNaOHШмвКЃЛЂм0.001mol/LЕФNaOHШмвК
AЃЎ1:10:100:1000ЁЁЁЁЁЁ ЁЁЁЁBЃЎ0:1:12:11ЁЁЁЁЁЁЁЁЁЁ CЃЎ14:13:12:11ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁD. ЁЁ14:13:2:3
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com