
题目列表(包括答案和解析)
7.pH相同的盐酸溶液和醋酸溶液分别与锌反应,若最后锌都全部溶解,且放出的气体一样多,则下列判断中正确的是( A )
A.整个反应阶段平均速率:醋酸>盐酸 B.反应所需的时间:盐酸=醋酸
C.开始反应时的速率:盐酸>醋酸 D.参加反应的锌的质量:盐酸<醋酸
6.25℃时,某水溶液中由水电离的c(H+)=10-10mol/L,则该溶液不可能是( D )
A.NaOH溶液 B.盐酸 C.氨水 D.FeCl3溶液
5.下列方程式属于电离方程式,并且正确的是( A )
A.HClO4 = H++ClO4- B.H2CO3 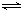 2H++CO32-
2H++CO32-
C.HCO3- + H2O
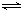 H2CO3
+ OH- D.NH3·H2O = NH4++OH-
H2CO3
+ OH- D.NH3·H2O = NH4++OH-
4.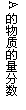
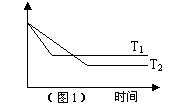 同压、不同温度下的反应:A(g)+B(g)
同压、不同温度下的反应:A(g)+B(g)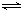 C(g),A的含量和温度的关系如图1所示,下列结论正确的是( C )
C(g),A的含量和温度的关系如图1所示,下列结论正确的是( C )
A.T1>T2,正反应吸热 B.T1<T2,正反应吸热
C.T1>T2,正反应放热 D.T1<T2,正反应放热
3.合成氨工业采用下列措施是为了使平衡正向移动而提高反应物转化率的是( B )
A.采用高温 B.采用高压 C.使用催化剂 D.以上均不对
2.可逆反应A+3B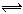 2C+2D,在4种不同情况下的反应速率分别为:
2C+2D,在4种不同情况下的反应速率分别为:
①VA=0.15mol/(L·s) ②VB=0.6mol/(L·s) ③VC=0.4mol/(L·s) ④VD=0.45mol/(L·s),该反应进行速率最快的是( D )
A. ① B. ② C. ③ D. ④
1.一密闭烧瓶中装有NO2气体,在一定条件下达到化学平衡2NO2 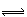 N2O4
(正反应为放热反应)。将该烧瓶放在热水中,则( C )
N2O4
(正反应为放热反应)。将该烧瓶放在热水中,则( C )
A.颜色不变 B.颜色变浅 C.颜色加深 D.无法判断
19. 元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)第四周期过渡元素的明显特征是形成多种多样的配合物。
① CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的二价阴离子为 (填电子式)。
② 金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 。
a. 水 b. 四氯化碳 c. 苯 d. 硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 。
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是
。
a.直线形;三角锥形 b.V形;三角锥形
c.直线形;平面三角形 d.V形;平面三角形
18. “嫦娥一号”登月成功,实现了中国人“奔月”的梦想。
(1)“嫦娥一号”使用的推进剂是液氢和液氧,这种推进剂的优点是
; 。(请写两条)
(2)下列是298K时,氢气(H2)、碳(C)、辛烷(C8H18)、甲烷(CH4)燃烧的热学化方程式:
H2(g)+1/2O2(g) H2O(l);△H=-285.8kJ/mol
C(g)+O2(g)CO2
(g);△H=-393.5kJ/mol
C8H18(l)+25/2O2(g) 8CO2(g)+9H2O(l);△H=-5518kJ/mol
CH4(g)+2O2(g) CO2(g)+2H2O(l);△H=-890.3kJ/mol
相同质量的H2、C、C8H18、CH4完全燃烧时,放出热量最多的是 ,通过计算说明等质量的氢气和碳燃烧时产生热量的比是 (保留1位小数)。
(3)已知:H2(g)=H2(l);△H=-0.92kJ/mol O2(g) O2(l);△H=-6.84kJ/mol
H2O(l)=H2O(g);△H=+44.0kJ/mol
请写出液氢和液氧生成气态水的热化学方程式: 。
如果此次嫦娥一号所携带的燃料为45吨,液氢、液氧恰好完全反应生成气态水,
总共释放能量 kJ(保留3位有效数字)。
(4)氢气、氧气不仅燃烧时能释放热能,二者形成的原电池还能提供电能,美国的探月飞船“阿波罗号”使用的就是氢氧燃料电池,电解液为KOH溶液,其电池反应式为:负极: ; 正极: ;
总反应式: 。
(5)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)=0.3mol·L-1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体。(写出计算过程)
①若溶液体积仍为100mL,此时溶液的pH为多少?(不考虑硫酸铜水解)
②此时氢氧燃料电池中消耗H2和O2的质量各是多少?(保留2位小数)
17. 目前用于抗幽门螺旋杆菌的常见高效抗生素是氨苄青霉素,它可由青霉素来合成。
目前用于抗幽门螺旋杆菌的常见高效抗生素是氨苄青霉素,它可由青霉素来合成。
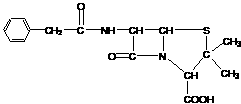
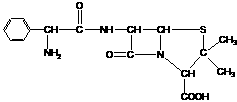
青霉素(C16H18N2O4S) 氨苄青霉素(C16H19N3O4S)
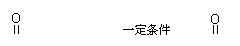
已知:…-C-NH-…+H2O
 …-C-OH+H2N-…
…-C-OH+H2N-…
下图是青霉素制取氨苄青霉素的合成路线:
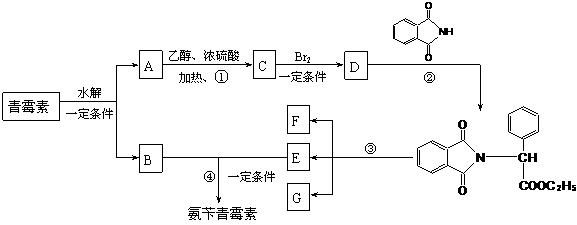
请回答下列问题:
⑴写出反应①②③④的反应类型
① , ② , ③ , ④ ;
⑵写出D的结构简式 ;
⑶写出反应①③的化学方程式:
① ,
③ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com