
题目列表(包括答案和解析)
15.下列离子方程式中,书写正确的是
A.铝片和氢氧化钠溶液反应: Al+2OH-=AlO2-+H2↑
B.硫酸镁溶液跟氢氧化钡溶液反应: SO4-+Ba+=BaSO4↓
C.硝酸亚铁溶液中加入少量的盐酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑
D.Fe2(SO4)3的酸性溶液中通入足量硫化氢 Fe3++H2S=Fe2++S↓+2H+
14.设NA表示阿伏加德罗常数,下列叙述中正确的是
A.1mol铜与足量硫充分反应后转移的电子数为2NA
B.100mL 0.5mol·L-1乙酸溶液中含乙酸分子数为0.05NA
C.常温常压下,31g白磷分子中的共价键数为6NA
D.标准状况下,2.24L二氧化碳与二氧化硫的混合气体中所含分子数为0.1NA
13.浓度均为0.1mol·L-1的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是:
A.BaCl2 NaOH NaHCO3 B.Na2CO3 MgCl2 H2SO4
C.AlCl3 NH3·H2O NaOH D.Ba(OH)2 CaCl2 Na2SO4
12.等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是
A.2mol·L-1H2SO4溶液 B.18 mol·L-1H2SO4溶液
C.6 mol·L-1KOH溶液 D.3 mol·L-1HNO3溶液
11.温度相同、浓度均为0.2 mol L-1的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、⑤CH3COONa溶液,它们的pH值由小到大的排列顺序是
A.③①④②⑤ B.①③④②⑤ C.③②①④⑤ D.⑤②④①③
10.下列有关滴定操作的正确顺序是:
(1)用标准溶液润洗滴定管 (2)往滴定管内注入标准溶液 (3)检查滴定管是否漏水 (4)滴定 (5)洗涤
A、(3)(1)(2)(4)(5) B、(3)(5)(1)(2)(4)
C、(3)(5)(2)(4)(1) D、(5)(1)(2)(4)(3)
9.室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是
A 0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液
B.0.1mol/L的硫酸和0.1mol/L的氢氧化钡溶液
C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液
D.pH=4的盐酸和pH=l0的氨水
8.pH=9 的Ba(OH)2溶液与pH=12的KOH溶液,按4:1的体积比混合,则混合溶液中H+浓度为(单位:mol·L-1)
A.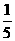 ×(4×10-9+1×10-12)
B.
×(4×10-9+1×10-12)
B.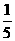 ×(8×10-9+1×10-12)
×(8×10-9+1×10-12)
C.5×10-10 D.5×10-12
7.我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为: 4Al+3O2+6H2O=
4Al(OH)3,下列说法不正确的是
A.正极反应为:O2+2H2O+4e-=4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需要更换铝板就可继续使用
6.某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)
Z(g)+W(s);ΔH>0下列叙述正确的是
A.加入少量W,逆反应速率增大
B.当容器中气体压强不变时,反应达到平衡
C.升高温度,平衡逆向移动
D.平衡后加入X,上述反应的ΔH增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com