
题目列表(包括答案和解析)
25.(10分)在某温度下,分别向容积相等的甲、乙两容器中通入0.6molN2O4气体,立即出现红棕色,此反应为吸热反应。反应过程中,甲容器保持体积不变,乙容器保持压强不变。乙容器达到平衡时,混合气体中各物质的物质的量相等。请回答下列问题:
(1)容器中气体出现红棕色的原因是(用化学方程式表示)___________________;
(2)反应达到平衡时,两容器中所需要的时间:甲______乙(填“大于”、“小于”或“等于”);
(3)乙容器中反应达到平衡时,N2O4的转化率是_______________;
(4)若使甲、乙两容器中反应达到平衡时,N2O4的浓度相等,不能采取的措施是(填序号)_____;
A.保持温度不变,适当压缩乙容器的体积
B.保持容器体积不变,适当升高甲容器的温度
C.保持容器体积不变,向甲容器中通入适量的N2O4
(5)若保持温度不变,乙容器起始时NO2的物质的量为0.4mol,达到平衡时,NO2的物质的量为0.8mol,混合气体中各物质的物质的量仍相等,则起始时容器中N2O4物质的量为________________;
24.(7分)为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。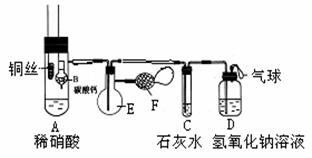
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先排出去其中的空气。你第一步实验操作为:__________________;
确定E中空气已被赶尽的实验现象为:______________________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子方程式为 ;
(3)如何证明E中收集到的是NO而不是H2?
________________________________________________________一段时间后,C中白色沉淀溶解,其原因是_____________ ;
(4)装置D的作用是_____________________________________。
23. (7分)下图中A-G是化合物,H是一种无色气态单质,D常温下是一种无色液体,E是一种淡黄色固体,它们有如下转化关系:
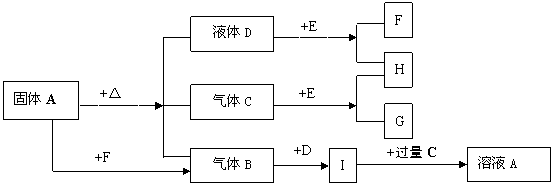
(1)写出A的名称:_________;B分子的空间构型为:____________;
C电子式:____________;
(2)C与E反应的化学方程式:______________________________________;
(3)固体A受热反应的化学方程式:___________________________________。
22.(8分)(1)在25℃条件下将pH=3的醋酸溶液稀释100倍,稀释后溶液的pH为(填序号)__________;
A.3 B.5 C.2~3之间 D.3~5之间
(2)25℃时,向0.1mol·L-1的醋酸溶液中加入少量醋酸钠晶体,当晶体溶解后测得溶液pH增大,主要原因是_______ ;
(3)室温下,向0.1mol·L-1的H2SO4中加入足量的锌粒,若想减慢制取H2的速率,但又不影响H2的体积,可以向硫酸溶液中加入 试剂;
(4)常温下,0.1mol·L-1的醋酸和PH=1的醋酸各100mL分别与足量的锌粒反应,产生的气体体积前者比后者 (填“大” ,“小” 或“等”)。
21.(4分)铵盐与碱反应均能生成氨气,写出实验室利用此原理制取氨气的反应的化学方程式____________________________;利用相同的发生装置还可制取_______________(填一种气体的分子式),简述如何检验集气瓶氨气是否已收集满了_______________________________。
20. 向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体。所得溶液中加入KSCN溶液无血红色出现,混合物中铁元素的质量分数为( )
A. 68.6% B. 77.8% C. 81.4% D. 无法计算
第II卷(共40分)
19. 在一定温度下,A2(g)+B2(g) 2AB(g)达到平衡的标志是:( )
在一定温度下,A2(g)+B2(g) 2AB(g)达到平衡的标志是:( )
A.单位时间内减少n mol A2,同时生成2n mol AB
B.单位时间内生成n mol B2,同时生成n mol AB
C.单位时间内生成 2xmol AB, 同时生成xmol A2
D.容器内各组成成分的物质的量之和不随时间变化而变化
18. 下列离子方程式正确的是
A.
苏打溶液中滴入少量稀盐酸: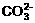 +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
B. 漂白粉溶液中通入过量CO2:Ca2++ 2ClO-+CO2+H2O=2HClO+ CaCO3↓
C.
三氯化铁溶液中滴入过量氨水:Fe3++3NH3·H2O=Fe(OH)3↓+3
D. 稀硝酸中加入少量铁粉:3Fe+ 4H++2NO3-= 3Fe2++2NO↑+ 2H2O
17. 对于反应mA(g)+nB(g)
pC(g)+qD(g) 满足下列图象,根据图象判断四种关系正确的是( )
对于反应mA(g)+nB(g)
pC(g)+qD(g) 满足下列图象,根据图象判断四种关系正确的是( )

A.m+n>p+q,正反应吸热 B. m+n<p+q, 正反应放热
C.m+n>p+q,正反应放热 D. m+n<p+q, 正反应吸热
16.向20mL2mol/LAlCl3溶液中加入30mLNaOH溶液,充分反应后得到0.78g白色沉淀,则NaOH溶液的物质的量浓度可能为( )
A.1.5 mol/L B. 2mol/L C. 5mol/L D. 8mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com