
题目列表(包括答案和解析)
8.下列关于丙烯(CH3-CH =CH2)的说法正确的是
A.丙烯分子有8个δ键,1 个∏键
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子不存在非极性键
D.丙烯分子中3个碳原子可能在同一直线上
7.下列说法中正确的是
A.处于最低能量的原子叫做基态原子
B.3p2表示3p能级有两个轨道
C.同一原子中,1s、2s、3s电子的能量逐渐减小
D.同一原子中,2p、3p、4p能级的轨道数依次增多
6.下列分子中,所有原子都满足8电子结构的是
A.六氟化硫 B.光气(COCl2)
C.二氟化氙 D.三氟化硼
5.具有下列电子排布式的原子中,半径最大的是
A.ls22s22p63s23p3 B.1s22s22p3
C.1s22s22p4 D.1s22s22p63s23p4
4.下列关于元素第一电离能的说法不正确的是
A.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠
B.因同周期元素的原子半径从左到右逐渐减小,故第一电离能必定依次增大
C.最外层电子排布为ns2np6(若只有K层时为1s2)的原子,第一电离能较大
D.对于同一元素而言,原子的逐级电离能越来越大
3.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢。它的分子构型是三角锥形。以下关于PH3的叙述正确的是
A.PH3分子中有未成键的孤对电子 B.PH3是非极性分子
C.PH3是一种强氧化剂 D.PH3分子的P-H键是非极性键
2.有关化学用语正确的是
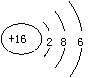 A.Cl-的电子排布式:1s22s22p63s23p6
B.乙醇的结构简式:C2H6O
A.Cl-的电子排布式:1s22s22p63s23p6
B.乙醇的结构简式:C2H6O
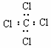
C.硫离子的结构示意图: D.四氯化碳的电子式:
1.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪种原子不能产生NMR现象
A.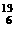 C
B.
C
B.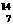 N
C.
N
C.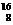 O
D.
O
D.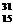 P
P
30.
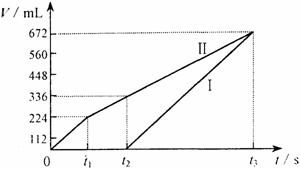 (8分)常温下电解200 mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如右图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:
(1)原混合溶液NaCl和CuSO4的物质的量浓度。
(2)t2时所得溶液的c(H+)。
(3)电解至t3时,消耗水的质量。
(8分)常温下电解200 mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如右图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:
(1)原混合溶液NaCl和CuSO4的物质的量浓度。
(2)t2时所得溶液的c(H+)。
(3)电解至t3时,消耗水的质量。
29.
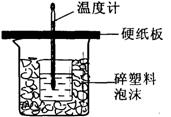 (10分)某同学利用如图所示的装置进行中和热测定的实验,实验步骤如下:
①在大烧杯底部垫碎泡沫塑料,放入小烧杯,再在大、小烧杯之间填上碎纸条,大烧杯上用硬纸板作盖板;
②用一个量筒取50mL2.0 mol·L-1盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,然后把温度计上的酸用水冲洗干净;
③用另一个量筒取50mL2.0 mol·L-1NaOH溶液,并用温度计测量NaOH溶液的温度;
④把套有盖板的温度计放入小烧杯的盐酸中,并将量筒中的NaOH溶液缓缓倒入小烧杯中(注意不要洒在外面),盖好盖板。用温度计轻轻搅动溶液(注意不要碰到烧杯底部或烧杯壁),并迅速读取混合溶液的温度,记为终止温度;
⑤________________________________________________________________________;
⑥根据实验数据计算中和热。
回答下列问题:
(1)请将上面第⑤步的实验步骤补充完整。
(2)从实验装置上看,图中尚缺少的一种玻璃仪器是(量筒除外)__________________。
(3)为保证该实验成功采取了许多措施,其中最主要的作用在于____________________。
(4)在以上①~④步操作或装置图中,有许多不当之处,请指出其中的四处:
Ⅰ
;Ⅱ
;
Ⅲ
;Ⅳ
;(5)用正确的方法测得含有11.2g KOH的稀溶液与1L0.1 mol·L-1的H2SO4溶液反应,放出11.46KJ热量,该反应的中和热化学方程式是__________________________________。
(10分)某同学利用如图所示的装置进行中和热测定的实验,实验步骤如下:
①在大烧杯底部垫碎泡沫塑料,放入小烧杯,再在大、小烧杯之间填上碎纸条,大烧杯上用硬纸板作盖板;
②用一个量筒取50mL2.0 mol·L-1盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,然后把温度计上的酸用水冲洗干净;
③用另一个量筒取50mL2.0 mol·L-1NaOH溶液,并用温度计测量NaOH溶液的温度;
④把套有盖板的温度计放入小烧杯的盐酸中,并将量筒中的NaOH溶液缓缓倒入小烧杯中(注意不要洒在外面),盖好盖板。用温度计轻轻搅动溶液(注意不要碰到烧杯底部或烧杯壁),并迅速读取混合溶液的温度,记为终止温度;
⑤________________________________________________________________________;
⑥根据实验数据计算中和热。
回答下列问题:
(1)请将上面第⑤步的实验步骤补充完整。
(2)从实验装置上看,图中尚缺少的一种玻璃仪器是(量筒除外)__________________。
(3)为保证该实验成功采取了许多措施,其中最主要的作用在于____________________。
(4)在以上①~④步操作或装置图中,有许多不当之处,请指出其中的四处:
Ⅰ
;Ⅱ
;
Ⅲ
;Ⅳ
;(5)用正确的方法测得含有11.2g KOH的稀溶液与1L0.1 mol·L-1的H2SO4溶液反应,放出11.46KJ热量,该反应的中和热化学方程式是__________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com