
题目列表(包括答案和解析)
6.新兴大脑营养学研究表明:大脑的发育与生长与不饱和脂肪有密切的联系,从深海鱼油中提取的被称作“脑黄金”的DHA就是一种不饱和程度很高的脂肪酸,它的分子中含6个碳碳双键,化学名称为:二十六碳六烯酸,它的分子组成应是 ( )
A.C25H50COOH B.C25H39COOH C.C26H41COOH D.C26H47COOH
5.已知A物质的分子结构简式如下: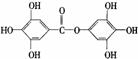 , lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
, lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
A.6mol B.7mol C.8mo1 D.9mo1
4.将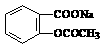 转变为
转变为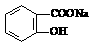 的方法为:( )
的方法为:( )
A.与足量的NaOH溶液共热后,再通入CO2 B.溶液加热,通入足量的HCl
C.与稀H2SO4共热后,加入足量的Na2CO3 D.与稀H2SO4共热后,加入足量的NaOH
3.有下列几种反应类型:①消去②加聚③水解④加成⑤还原⑥氧化,用丙醛制取1,2一丙二醇,按正确的合成路线依次发生的反应所属类型应是 ( )
A.⑤①④③ B.⑥④③① C.①②③⑤ D.⑤③④①
2.下列说法中错误的是 ( )
A.C2H6和C4H10一定是同系物
B.在相同条件下,燃烧等物质的量的C2H4和乙醇,消耗O2体积相同
C.相对分子质量相同的两种物质一定是同分异构体
D.烯烃各同系物中碳的质量分数都相等
1.下列各组物质的最简式相同的是( ) A.乙酸和乙二酸 B.丁酸和乙酸 C.甲醛和乙酸 D.乙二酸和乙二醇
22.(13分)钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
(1)钛有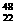 Ti和
Ti和 Ti两种原子,它们互称为
。Ti元素在元素周期表
Ti两种原子,它们互称为
。Ti元素在元素周期表
中的位置是第 周期,第 族;基态原子的电子排布式
为 ;按电子排布Ti元素在元素周期表分区中属于 区元素
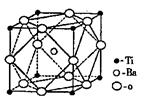 (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛
酸钡晶体中晶胞的结构如右图所示,它的化学式是
(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2·H2O。配
离子[TiCl(H2O)5]2+中含有的化学键类型是 、
该配合物的配体是 、 。
21.(9分)现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
T |
M层上有2对成对电子 |
|
X |
最外层电子数是次外层电子数的2倍 |
|
Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
|
Z |
元素最高正价是+7价 |
(1)元素T的原子最外层共有 种不同运动状态的电子。元素X的一种同位素可测定文物年代,这种同位素的符号是
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式
(3)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a 常温下Z的单质和T的单质状态不同
b Z的氢化物比T的氢化物稳定
c 一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是 ,
理由是
20.(12分)下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:
|
a |
|
|
|||||||||||||||
|
|
|
|
|
f |
|
h |
i |
|
|||||||||
|
|
b |
|
e |
|
|
|
j |
|
|||||||||
|
c |
|
|
|
|
|
|
d |
|
|
|
|
|
g |
|
|
k |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l |
|
(1)请写出上述元素d3+的核外电子排布式 ;
(2)请写出j的单质与a、h形成的化合物发生反应的化学方程式 ;
(3)请比较b、e、j三种元素的电负性由大到小的顺序 (写元素符号);此三种元素的第一电离能由大到小的顺序 (写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水合物与a、c、h三种元素形成的化合物反应的离子方程式 ;
(5)j、k、l三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素单质的性质。请写出k、l的互化物的电子式 ,它是由 键(根据原子轨道的重叠程度填写)形成的 化合物(填“离子”或“共价”)。
19.(6分)Co(NH3)5BrSO4可形成两种钴的配合物 ,已知Co3+ 的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2 溶液时,产生白色沉淀,在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的结构式为 ,第二种配合物的结构式为 ,如果在第二种配合物溶液中滴加AgNO3溶液时,产生 现象。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com