
题目列表(包括答案和解析)
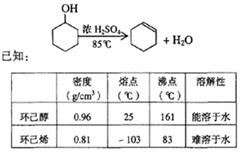
21.(10分)某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
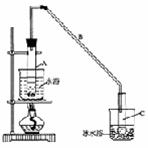
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________。
②试管C置于冰水浴中的目的是____________。
(2)制备精品
 ①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
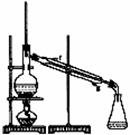
②再将环己烯按右图装置蒸馏,冷却水 从_________口进入。蒸馏时要加入生石灰,目的是_____________。
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是( )
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
20.下列分离或提纯物质的方法错误的是( )
A.用渗析的方法精制氢氧化铁胶体
B.用溶解、过滤的方法提纯含有少量硫酸钡的碳酸钡
C.用加热的方法提纯含有少量碳酸氢钠的碳酸钠
D.用盐析的方法分离、提纯蛋白质
19.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是( )
A.K+一定存在
C.Cl-不可能存在
B.100mL溶液中含0.01mol CO32-
D.Ba2+一定不存在,Mg2+可能存在
18.用惰性电极电解饱和食盐水100mL,经过一段时间后,阴极收集到112 mL氢气(标准状况),此时电解液的pH为(电解液的体积保持不变)( )
A.13
B.12
C.8
D.1
17.已知常温常压下饱和CO2溶液的pH值约为3.9,则可以推断盐酸滴定NaHCO3溶液测定其浓度时,适宜选用的指示剂及其终点的颜色变化是( )
A.石蕊,由蓝变红
C.甲基橙,由橙变黄
B.酚酞,红色褪去
D.甲基橙,由黄变橙
16.如图所示,下列叙述正确的是( )
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X为滤纸接触处变红
15.用惰性电极电解1L 0.1mol·L-1含Cu2+、X3+的水溶液,阴极增重量与通过电子的物质的量的关系如图所示,则溶液中离子的氧化性有强到弱的顺序是( )
A.Cu2+>X3+>H+
B.X3+ > Cu2+>H+
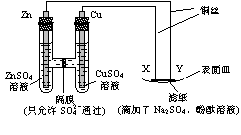 C.Cu2+>H+>X3+
C.Cu2+>H+>X3+
D.H+>Cu2+>X3+
14.钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2 =2Fe2++4OH-。以下说法正确的是( )
A.负极发生的反应为:Fe-2e- = Fe2+
 B.正极发生的反应为:2H2O+O2+2e-=4OH-
B.正极发生的反应为:2H2O+O2+2e-=4OH-
C.原电池是将电能转变为化学能的装置
D.钢柱在水下部分比在空气与水交界处更容易腐蚀
13.一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);DH<0。现将1
mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g);DH<0。现将1
mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
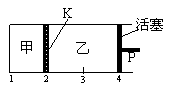

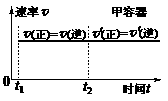
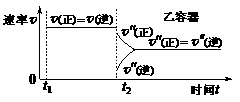
图1 图2 图3
A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
12.CuS和Cu2S都能溶于硝酸,它们高温灼烧的产物相同,以下鉴别CuS和Cu2S两种黑色粉末的方法合理的是( )
A.将两种样品分别溶于硝酸,区别所产生的气体
B.将两种样品分别溶于硝酸,区别溶液的颜色
C.取两种同质量的样品分别在高温灼烧,区别残留固体的质量
D.取两种同质量的样品分别在高温灼烧,区别残留固体的颜色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com