
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
6ЁЂЯТСаЪТЪЕгыЧтМќгаЙиЕФЪЧ(ЁЁЁЁ )
ЁЁ ЂйNH3взвКЛЏЃЛЂкбѕзхдЊЫиЕФЧтЛЏЮяжаЃЌH2OЕФЗаЕузюИпЃЛЂлТБзхдЊЫиЕФЧтЛЏЮяжаЃЌHFЕФЮШЖЈадзюЧПЃЛЂмБљЕФУмЖШБШЫЎаЁЃЛЂнH2SЕФЛЙдадЧПгкH2O
ЁЁ AЁЂЂйЂкЂлЁЁЁЁ BЁЂЂйЂкЂмЁЁЁЁЁЁ CЁЂЂйЂкЂлЂмЁЁЁЁЁЁ DЁЂШЋВП
5ЁЂЯТСаа№Ъіе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁ AЁЂдзгОЇЬхЖМЪЧЕЅжЪЃЌОЇЬхжажЛКЌгаЙВМлМќ
ЁЁ BЁЂРызгОЇЬхЖМЪЧЛЏКЯЮяЃЌОЇЬхжажЛКЌгаРызгМќЃЌВЛКЌгаЙВМлМќ
ЁЁ CЁЂЗжзгОЇЬхМШгаЕЅжЪгжгаЛЏКЯЮяЃЌОЇЬхжажЛДцдкЗжзгМфзїгУСІЃЌВЛКЌгаЦфЫћЛЏбЇМќ
ЁЁ DЁЂН№ЪєОЇЬхЖМЪЧЕЅжЪЃЌОЇЬхжаКЌгабєРызгЃЌЕЋВЛКЌгавѕРызг
4ЁЂЯТСаИїзщЮяжЪжаЃЌЛЏбЇМќРраЭЯрЭЌЃЌОЇЬхРраЭвВЯрЭЌЕФЪЧ(ЁЁЁЁ )
ЁЁ AЁЂC(Н№ИеЪЏ)КЭCO2ЁЁЁЁЁЁЁЁЁЁЁЁ BЁЂNaBrКЭHBr
ЁЁ CЁЂCH4КЭH2OЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЁЂNa2O2КЭH2O2
3ЁЂЯТСаИпЗжзгВФСЯгыЦфгУЭОЖдгІЙиЯЕВЛе§ШЗЕФЪЧ(ЁЁЁЁ )
|
ЁЁ |
ВФСЯ |
гУЭО |
|
A |
ОлввЯЉ |
ЪГЦЗДќЁЂАќзАДќ |
|
B |
КЯГЩЯ№НК |
Я№ЦЄЙмЁЂТжЬЅ |
|
C |
ЙшОлКЯЮяЁЂОлАБѕЅ |
ШЫЙЄаФдрЕШШЫдьЦїЙй |
|
D |
ВЃСЇИж |
ИпЧПЖШЕМЕчВФСЯ |
2ЁЂ2008ФъББОЉАТдЫЛсЁАЯщдЦЁБЛ№ОцгУЕФЪЧЛЗБЃаЭШМСЯ--БћЭщЁЃвбжЊБћЭщЕФШМЩеШШЮЊЁЁЁЁЁЁЁЁЁЁ 2221.5 KJ/molЃЌЯТСагаЙиЫЕЗЈВЛе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁ AЁЂБћЭщЕФЗаЕуБШе§ЖЁЭщЕЭ
ЁЁ BЁЂАТдЫЛ№ОцШМЩежївЊЪЧНЋЛЏбЇФмзЊБфЮЊШШФмКЭЙтФм
ЁЁ CЁЂБћЭщЁЂПеЦјМАВЌЦЌПЩзщГЩШМСЯЕчГиЃЌдкБћЭщИННќЕФВЌМЋЮЊЕчГиЕФе§МЋ
ЁЁ DЁЂБћЭщШМЩеЕФШШЛЏбЇЗНГЬЪНЮЊC3H8(g)+5O2(g)====3CO2(g)+4H2O(1)ЃЛ
 2 221.5 kJ/mol
2 221.5 kJ/mol
1ЁЂЯТСаа№ЪіЃЌДгЛЏбЇНЧЖШЗжЮіе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁ AЁЂФОВФЁЂУоЛЈЁЂбђУЋЁЂФсСњЖМЪєгкЬьШЛЯЫЮЌЃЌЖјНѕТкЁЂЬМЯЫЮЌЁЂЙтЕМЯЫЮЌдђЪєгкКЯГЩЯЫЮЌ
ЁЁ BЁЂУКЦјЛЏММЪѕЕФЪЙгУЃЌЫфШЛФмДяЕНМѕЩйЖўбѕЛЏСђКЭбЬГОХХЗХЕФФПЕФЃЌЕЋВЛФмЬсИпУКЕФШМЩеаЇТЪ
ЁЁ CЁЂЪГгУжВЮягЭЕФжївЊГЩЗжЪЧИпМЖБЅКЭжЌЗОЫсИЪгЭѕЅЃЌЪЧШЫЬхЕФгЊбјЮяжЪ
ЁЁ DЁЂИФНјЫмСЯЕФХфЗНКЭЩњВњЙЄвеЃЌбаОППЊЗЂвзЗжНтЕФаТаЭЫмСЯЃЌШчЕэЗлЫмСЯЁЂЫЎШмЫмСЯЁЂЙтНтЫмСЯЕШЪЧжЮРэЁААзЩЋЮлШОЁБЕФЗЂеЙЗНЯђ
26ЁЂ(6Зж)дкЮТЖШЮЊ373KЪБЃЌАб11.5g N2O4ЦјЬхЭЈШыЬхЛ§ЮЊ500mlЕФецПеУмБеШнЦїжаСЂМДГіЯжКьзиЩЋЃЌЗДгІНјааЕН2sЪБЃЌNO2КЌСПЮЊ0.01molЃЌНјааЕН60sЪБЃЌДяЕНЦНКтЃЌДЫЪБШнЦїжаЛьКЯЦјЬхЕФУмЖШЪЧЧтЦјУмЖШЕФ28.75БЖЃЌдђЃК
ЂХПЊЪМЪБ2sФквдc(N2O4)ЕФБфЛЏБэЪОЕФЗДгІЫйТЪЪЧЖрЩй?
ЂЦДяЕНЦНКтЪБЬхЯЕФкЕФбЙЧПЪЧПЊЪМЕФЖрЩйБЖ?
ИпвЛЛЏбЇЪдЬтЁЁЁЁ (ЙВ8вГ)ЁЁЁЁЁЁ Ек8вГ
25ЁЂ(6Зж)ЯђвЛЖЈбЙЕФвЧЦїжаГфШы4LN2КЭH2ЕФЛьКЯЦјЬхЃЌЗДгІКѓЛжИДЕНдЮТЖШЃЌ ЬхЛ§БфЮЊ3.4LЃЌШнЦїФкЦјЬхЖдЯрЭЌЬѕМўЯТH2ЕФЯрЖдУмЖШЮЊ5ЁЃ
ЂХЗДгІДяЕНЦНКтЪБV(NH3)=ЁЁЁЁЁЁЁЁЁЁЁЁ LЃЌ
ЗДгІЧАV(N2)ЃКV(H2)=ЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌN2ЕФзЊЛЏТЪЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЦЯђЦНКтКѓЕФШнЦїжадйГфШы0.2molNH3ЃЌдйДяЕНЦНКтЃЌВтЕУЮќЪеСЫ6.44kJЕФШШСПЁЃ
ЂйДгПЊЪМЕНжиаТЦНКтЃЌЛьКЯЦјЬхЖдH2ЕФЯрЖдУмЖШБфЛЏЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁAЁЂЯШдіДѓКѓБфаЁЁЁЁЁ BЁЂЯШМѕаЁКѓдіДѓЁЁ CЁЂвЛжБМѕаЁЁЁЁЁ DЁЂвЛжБВЛБф
ЂкаДГіКЯГЩАБЕФШШЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
24ЁЂ(11Зж)ЪЕбщЪвгУ50mL 0.50mol/LЕФбЮЫсгы50mL 0.55mol/LЕФЩеМюШмвКНјааЗДгІЃЌЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЕФЗХШШРДМЦЫужаКЭШШЁЃЪдЛиД№ЯТСаЮЪЬтЃК
(1)дкБОЪЕбщжаГ§СЫгУЕНДѓЩеБЁЂаЁЩеБЁЂЮТЖШМЦЁЂСПЭВЕШвЧЦїЭтЃЌЛЙаыЕФвЛжжВЃСЇвЧЦїУћЮЊ______________________ЁЃ
(2)СНжЛЩеБМфвЊЬюТњЫщжНЬѕЃЌЦфФПЕФЪЧ________________________ЃЛ
(3)ДѓЩеБЩЯБиаыИЧЩЯгВжНАхЃЌЗёдђЃЌЧѓЕУЕФжаКЭШШЪ§жЕНЋ____________(ЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЁЂЁАЮогАЯьЁБ)ЁЃ
(4)ЪЕбщЪБЫљгУбЮЫсМАNaOHШмвКЕФЬхЛ§ОљЮЊ50mLЃЌИїШмвКУмЖШЮЊ1g/cm3ЃЌЩњГЩШмвКЕФБШШШШнC ЃН4.18J/(gЁЄЁц)ЃЌЪЕбщЦ№ЪМЮТЖШЮЊt1ЁцЃЌжежЙЮТЖШЮЊt2ЁцЁЃЪдЭЦЖЯжаКЭШШЕФМЦЫуЪНЃКЁїHЃН________________ЁЃ
(5)ЪЕбщжаИФгУ52mL 0.50mol/LЕФбЮЫсгы50mL 0.55mol/LЕФЩеМюШмвКЗДгІЃЌгыЩЯЪіЪЕбщЯрБШЃЌЫљЗХГіЕФШШСП______________(ЬюЁАЯрЕШЁБЁАВЛЯрЕШЁБ)ЃЌЫљЧѓжаКЭШШ______________(ЬюЁАЯрЕШЁБЁАВЛЯрЕШЁБ)ЃЌМђЪіРэгЩ__________________________________________________________________________________________________________________________
(6)гУЯрЭЌХЈЖШКЭЬхЛ§ЕФАБЫЎДњЬцЩеМюШмвКНјааЩЯЪіЪЕбщЃЌВтЕУЕФжаКЭШШЕФЪ§жЕЛс__________ЃЛШєИФгУ50mL 0.50 mol/LЩеМюШмвКНјааЩЯЪіЪЕбщЃЌВтЕУЕФжаКЭШШЕФЪ§жЕЛс______________ЁЃ(ЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЁЂЁАЮогАЯьЁБ)
ИпвЛЛЏбЇЪдЬтЁЁЁЁ (ЙВ8вГ)ЁЁЁЁЁЁ Ек7вГ
23ЁЂ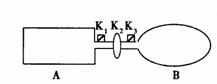 (7Зж)AЪЧгЩЕМШШВФСЯжЦГЩЕФУмБеШнЦїЃЌBЪЧвЛФЭЛЏбЇИЏЪДЧввзгкДЋШШЕФЦјЧђЁЃЙиБеK2ЃЌНЋЕШСПЧвЩйСПЕФNO2ЭЈЙ§K1ЁЂK3ЗжБ№ГфШЫAЁЂBжаЃЌЗДгІЦ№ЪМЪБЃЌAЁЂBЕФЬхЛ§ЯрЭЌЁЃ(вбжЊЃК2NO2ЁЁ
(7Зж)AЪЧгЩЕМШШВФСЯжЦГЩЕФУмБеШнЦїЃЌBЪЧвЛФЭЛЏбЇИЏЪДЧввзгкДЋШШЕФЦјЧђЁЃЙиБеK2ЃЌНЋЕШСПЧвЩйСПЕФNO2ЭЈЙ§K1ЁЂK3ЗжБ№ГфШЫAЁЂBжаЃЌЗДгІЦ№ЪМЪБЃЌAЁЂBЕФЬхЛ§ЯрЭЌЁЃ(вбжЊЃК2NO2ЁЁ  ЁЁЁЁN2O4ЃЛЁїH<0)
ЁЁЁЁN2O4ЃЛЁїH<0)
ЁЁ(1)вЛЖЮЪБМфКѓЃЌЗДгІДяЕНЦНКтЃЌДЫЪБAЁЂBжаЩњГЩЕФN2O4ЕФЫйТЪЪЧVA_________VBЁЃ(ЬюЁА>ЁБЁЂЁА<ЁБЁЂЁА=ЁБ)ЃЛШєДђПЊЛюШћK2ЃЌЦјЧђBНЋ__________(ЬюЃКБфДѓЁЂБфаЁЁЂВЛБф)ЁЃ
(2)ШєдкAЁЂBжадйГфШЫгыГѕЪМСПЯрЕШЕФNO2ЃЌдђДяЕНЦНКтЪБЃЌNO2ЕФзЊЛЏТЪ
ІСAНЋ_________ (ЬюдіДѓЛђМѕаЁЁЂВЛБф)ЃЛШєЭЈШЫЕШСПЕФNeЦјЃЌдђДяЕНЦНКт
ИпвЛЛЏбЇЪдЬтЁЁЁЁ (ЙВ8вГ)ЁЁЁЁЁЁ Ек6вГ
ЪБЃЌAжаNO2ЕФзЊЛЏТЪНЋ_________ЃЌBжаNO2ЕФзЊЛЏТЪНЋ_________(ЬюЃК
БфДѓЁЂБфаЁЁЂВЛБф)ЁЃ
(3)ЪвЮТЯТЃЌШєAЁЂBЖМБЃГжЬхЛ§ВЛБфЃЌНЋAЬзЩЯвЛИіОјШШВуЃЌBгыЭтНчПЩвдНјааШШДЋЕнЃЌдђДяЕНЦНКтЪБЃЌ_________жаЕФбеЩЋНЯЩюЁЃ
(4)ШєдкШнЦїAжаГфШЫ4.6gЕФNO2ЃЌДяЕНЦНКтКѓШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПЮЊ57.5ЃЌдђЦНКтЪБN2O4ЕФЮяжЪЕФСПЮЊ_________ЁЃЁЁЁЁЁЁ

АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com