
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
25. (11·Ц)
(1)ЎЎ ЎЎЎЎCl2ЎЎ ЎЎЎЎЈ¬ЎЎ ЎЎЎЎSO2ЎЎЎЎЎЎ ЎЎЈ¬ ЎЎЎЎNaClЎЎ ЎЎЎЎЎЎ(ёч1·Ц)ЎЈ
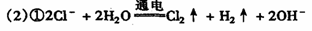 (2)CЎъE
(2)CЎъE
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ Ј»(2·Ц)
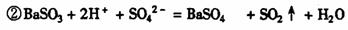 D+GЎъH
D+GЎъH
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ Ј»(2·Ц)
(3) ұдәмЙ«ЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(1·Ц)
ФӯТтКЗ ЎЎAОӘBaCl2Ј¬BОӘNa2SO3Ј¬ТтAУлBКЗөИОпЦКөДБҝ»мәП(Na2SO3+BaCl2ЈҪ2NaCl+BaSO3Ўэ)ЛщТФөзҪвNaClұҘәНИЬТәөГөҪөДCl2әНBaSO3УлH2SO4·ҙУҰЙъіЙөДSO2ТаОӘөИОпЦКөДБҝЈ¬јҙCl2УлSO2ЗЎәГНкИ«·ҙУҰЈәSO2+Cl2+2H2OЈҪ2HCl+H2SO4Ј¬ЧоЦХөГөҪCИЬТәЦ»УРЛбРФ¶шОЮЖҜ°ЧРФЎЈЎЎЎЎ (3·Ц)
24. (10·Ц)
I . (1)ЎЎ ·с ЎЎЎЎ(1·Ц)ЎЎ Ј»ЎЎЎЎ AB ЎЎЎЎЎЎЎЎ(2·Ц)ЎЈ(ИфХэИ·Ј¬ҙЛОКІ»ҙр)
(2) C ЎЎ(1·Ц)Ј»(3) ЎЎЎЎDЎЎ (1·Ц)Ј»(4) = (2·Ц)ЎЈ
IIЈ®(5) ЎЎ10-13»т1.0ЎБ10-13ЎЎ (1·Ц)ЎЈ(6)pH=ЎЎ ЎЎ12ЎЎ ЎЎЎЎЎЎЎЎ(2·Ц)ЎЈ
23Ўў(12·Ц)(1)ЎЎЎЎ ФцҙуЎЎЎЎЎЎ (2·Ц)
(2)ЎЎЎЎ KЦөФҪҙуЈ¬өзАліцөДЗвАлЧУЕЁ¶ИФҪҙуЈ¬ЛщТФЛбРФФҪЗҝЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (2·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(3) ЎЎH3PO4ЎЎЎЎЎЎ ЎЎЈ¬(2·Ц) ЎЎЎЎHPO42-ЎЎЎЎЎЎЎЎ (2·Ц)
(4) K1ЈәK2ЈәK3ЎЦ1Јә10-5Јә10-10 (ЎЎ »тҙр K1ЈҫЈҫK2ЈҫЈҫK3Ј¬ЎЎЎЎ »тҙрK1Ф¶ҙуУЪK2Ф¶ҙуУЪK3)Ј»(2·Ц)
КЗЎЎ ЙПТ»ј¶өзАлІъЙъөДH+¶ФПВТ»ј¶өзАлУРТЦЦЖЧчУГ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(2·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
22Ўў(10·Ц)
ўЕ AЎЎ Al2(SO4)3 Ј¬CЎЎ AlCl3 Ј¬DЎЎ AgClЎЎ Ј¬EЎЎ Ba(OH)2ЎЎ ЎЈўЖЎЎ BaSO4ЎЎЎЎЎЎЎЎЎЎ ЎЈ(ёч2·Ц)
21Ўў(15·Ц)
(1)ЎЎЎЎЎЎ 14HNO3+3Cu2OЈҪ6Cu(NO3)2+2NOЎь+7H2OЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎ(3·Ц)ЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(2)ЎЎЎЎ ЛбРФЎЎЎЎ (2·Ц)ЎўЎЎ Сх»ҜРФЎЎЎЎ ЎЎ(2·Ц)ЎЈ(3)ЎЎ 0.6molЎЎ molЎЈЎЎЎЎЎЎ (2·Ц)
(4)ЎЎ 14H++2NO3-+3Cu2OЈҪ6Cu2++2NOЎь+7H2OЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎ(3·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(5)ФӯТтКЗЈәК№УГБЛҪПЕЁөДПхЛбЈ¬ІъОпЦРУРІҝ·Ц¶юСх»ҜөӘЙъіЙЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎ(3·Ц)ЎЎЎЎЎЎЎЎЎЎ
20Ўў(5·Ц)(ГҝҝХ1·Ц)
(1)ЎЎ ЎЎЎЎ1Јә1ЎЎЎЎЎЎ Ј»(2) ЎЎЎЎ1Јә2 ЎЎЎЎЎЎЈ»(3) ЎЎЎЎЎЎ1Јә1ЎЎЎЎЎЎЎЎ Ј»
(4)ЎЎЎЎ 2Јә3 ЎЎЎЎЎЎЎЎЈ»(5)ЎЎ ЎЎ7Јә11ЎЎЎЎЎЎ ЎЈ
19Ўў(14·Ц)
(1)ЦГ»»·ҙУҰ ЎЎ2Al+6H+=2Al3++3H2Ўь»тЎЎ 2Al+3Cu2+=2Al3++3Cu ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(2·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
»ҜәП·ҙУҰЎЎ ЎЎ2Cu+O2+H2O+CO2=Cu2(OH)2CO3ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (2·Ц)ЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(2)ПЦПуКЗЎЎ ЎЎ°ЧЙ«іБөнЙъіЙ,әуіБөнЦрҪҘИЬҪвЦБПыК§ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (2·Ц) ЎЎЎЎЎЎЎЎЎЎ
КЗЎЎ ЎЎAl3++3OHЈӯ = Al(OH)3ЎэЎЎ ЎЎЎЎЈ»ЎЎЎЎ Al(OH)3+OHЈӯ = AlO2Јӯ+2H2OЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎ(4·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(3)ўЩ ЎЎЎЎ3MnO2+4Al = 3Mn+2Al2O3 ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(2·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎ
ЎЎЎЎ ўЪЎЎЎЎ ЎЎMnO2+H2O2+2H+ = Mn2++O2Ўь+2H2OЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (2·Ц)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎ
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
B |
D |
A |
D |
C |
B |
B |
B |
D |
|
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
D |
C |
D |
AD |
C |
D |
C |
AC |
D |
26Ј®(№І10·Ц)(1)ЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЈ
(2)BЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎCЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎ
КфУЪЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ·ҙУҰЎЈ
(3)ЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎ(4)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЈ
(5)
ЎЎ
ЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
2007-2008С§Дк¶ИөЪ¶юС§ЖЪРмОЕёЯ¶ю»ҜС§өЪ¶юҙОФВІвМвҙр°ё
25. (11·Ц)
(1)ЎЎЎЎЎЎ ЎЎЎЎЎЎЈ¬ЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЈ¬ЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
(2)
ЎЎCЎъEЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ Ј»
ЎЎD+GЎъHЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ Ј»
(3)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ¬
ФӯТтКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com