
题目列表(包括答案和解析)
10.(4分)有铁和三氧化二铁组成的粉末状混合物19.2g,向其中加入250mL未知浓度的稀硫酸,当固体全部溶解时,放出3.36L氢气(标准状况)。经测定,反应后的溶液中C(H+)为1.6mol/L,且溶液中不含三价铁离子,求:(l)混合物中铁和三氧化二铁的质量各为多少克?(2)所加稀硫酸的物质的量浓度是多少?(要求写出详细的解题过程)
9.(4分)将11.2L氢气和14.2g氯气混合,使其在光照条件下充分反应,并将生成的氯化氢全部溶于水制成250mL溶液。试计算(气体体积均在标准状况下测定):
(1)生成氯化氢的体积。
(2)所得溶液的物质的量浓度。
8.(6分)为分析某地区的空气质量状况,某校化学研究性学习小组的同学拟测定该地区空气中SO2的含量(假设分析过程中涉及的气体体积均为标况下气体体积)。
⑴ 检验SO2可选用 试液。
⑵ SO2与酸性KMnO4溶液反应的离子方程式为:
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+。该反应的现象是 ,
SO2在该反应中体现 (填“氧化”或“还原”)性。
⑶ 该小组的同学拟用下列装置运用“⑵”中的反应原理定量分析空气中SO2的含量:

① 装置中棉花的作用是 ,
通入空气前应进行的实验操作是 ;
② 该实验中需要知道的数据除气体流速、酸性KMnO4溶液的体积外还有 。
7.(4分)为测定由CO、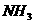 、
、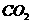 、
、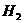 组成的混合气体中各成分的体积分数,请用下列装置设计一个简单实验(装置不能重复使用,所用试剂均过量)。
组成的混合气体中各成分的体积分数,请用下列装置设计一个简单实验(装置不能重复使用,所用试剂均过量)。
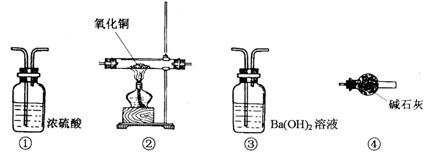
 已知存在下列反应:2NH3 + 3CuO 3Cu + N2
+ 3H2O
已知存在下列反应:2NH3 + 3CuO 3Cu + N2
+ 3H2O
请回答:
(1)混合气体通过各装置的顺序依次是( )→(①)→( )→( );
(2)写出装置③中有关反应的离子方程式_________ _________;
(3)装置③和④的位置不可互换,其原因是_______________ _________。
6.(3分)有下图所示的A、B、C、D、E五种仪器,请选择仪器的编号完成下列填空。
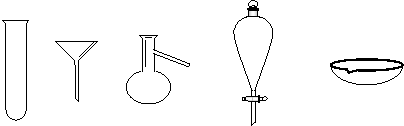
A B C D E
(1)可用酒精灯直接加热的有______________。
(2)分馏石油需用_____________。
(3)分离汽油和水的混合物需用____________。
5.(6分)已知A是黑色固体(常作燃料),B为常见的强酸,C和F是无色气体,D是红棕色气体,转化关系如下:
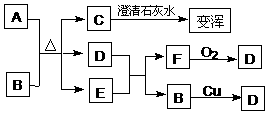
(1)请写出C的电子式 ,F的分子式 。
(2)请写出A和B反应的化学方程式: 。
(3)请写出D和E反应的离子方程式: 。
4.(7分)某同学为探究碳酸钠的性质,进行了如下实验,请你按要求回答有关问题。
(1)配制100 mL 0.5 mol/L的Na2CO3溶液。该同学用天平称量Na2CO3固体的质量为 g。在配制该溶液时,需要用到的玻璃仪器有 、 、 和 。
(2)用pH试纸检测所配溶液的pH,pH>7,说明Na2CO3溶液呈 (填“酸性”、“碱性”或“中性”);用试管取少量所配溶液,向溶液中滴加几滴酚酞试液,溶液变红,再用酒精灯加热,溶液的颜色变深,说明升高温度,对Na2CO3的水解有 作用。
3.(5分)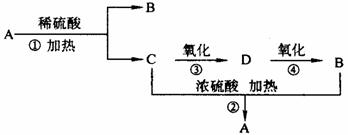 化合物A是一种酯,它的分子式为C4H8O2,有下图转化关系。试回答下列问题。
化合物A是一种酯,它的分子式为C4H8O2,有下图转化关系。试回答下列问题。
(1)A的名称是 。
(2)B的结构简式是 。
(3)D中含有的官能团是 (填名称)。
(4)写出B和C反应生成A的化学方程式 。
2.(5分)钠、铝和铁是三种重要的金属。请回答:
(1)三种金属中,常温下遇浓硫酸或浓硝酸不会发生钝化现象的是 (填化学式);三种金属中,某种金属的氢氧化物M 既能与强酸反应,又能与强碱溶液反应,请写出M与强碱溶液反应的离子方程式 。
(2)三种金属在一定条件下均能与水发生反应。其中铁与水蒸气在高温下反应的化学方程式为 ;钠与水反应时可观察到的实验现象有____________ (填字母)。
a.钠浮在水面上 b.钠熔成小球 c.钠四处游动 d. 溶液变为红色
1.(6分)在3517Cl原子中含有 个质子, 个中子;它的原子结构示意图为 。铁在氯气中燃烧,生成 (填化学式),在这个反应中,氯气是 剂(填“氧化”或“还原”)。在此反应中,每转移1.5mol电子,消耗的铁是 g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com