
题目列表(包括答案和解析)
21、(9分)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、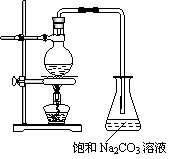 纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH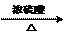 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)若用右图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为:__________________________、______________________________等。
(2)此反应以浓硫酸为催化剂,可能会造成____________、_________等问题。
(3)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
|
同一反应时间 |
同一反应温度 |
||||
|
反应温度/℃ |
转化率(%) |
选择性(%) |
反应时间/h |
转化率(%) |
选择性(%) |
|
40 |
77.8 |
100 |
2 |
80.2 |
100 |
|
60 |
92.3 |
100 |
3 |
87.8 |
100 |
|
80 |
92.6 |
100 |
4 |
92.3 |
100 |
|
120 |
94.5 |
98.7 |
6 |
93.0 |
100 |
|
选择性100%表示反应生成的产物是乙酸乙酯和水 |
①根据表中数据,下列__________(填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
②当反应温度达到120℃时,反应选择性降低的原因可能为__________。
(3)请设计实验方案进一步确定该固体混合物的组成。叙述实验操作、预期现象和结论。
[提示]Ⅰ、在答题卡上按以下方式作答,注意前后内容对应;
Ⅱ、注意文字简洁,确保不超过答题卡空间,可以不填满。
|
实验操作 |
预期现象和结论 |
|
|
|
|
|
|
20.(11分)向草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色总是先慢后快。对其原因,某研究性学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究:
实验(1):在2支试管中分别加入10mL等浓度的草酸溶液,在①号瓶中加入少量硫酸锰固体。然后在两支试管中加入0.1 mol·L-1的高锰酸钾溶液现象如下(表1)
|
加入药品 |
不加硫酸锰的硫酸酸化的草酸溶液 |
加少量硫酸锰的硫酸酸化的草酸溶液 |
|
实验现象(褪色时间) |
草酸褪色很慢(30s) |
草酸褪色很快(2s) |
实验(2):在2支试管中分别加入5 mL等浓度的草酸溶液,在②号试管中再滴加10滴稀硫酸,然后加入5滴0.1 mol·L-1的高锰酸钾溶液。现象如下(表2)
|
编号 |
①号试管 |
②号试管 |
|
褪色时间 现象 |
100
s |
90
s |
|
均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
实验(3):取3支试管分别加入5 mL等浓度草酸溶液,然后在①、②、③号试管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高锰酸钾溶液,然后置于温度为65℃的水浴中加热。观察现象(表3)。
|
编号 |
①号试管 |
②号试管 |
③号试管 |
|
褪色时间 实验现象 |
90
s |
100
s |
120
s |
|
均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
(1) 该研究性学习小组提出猜想与假设的理论依据是(从化学反应原理的角度作答): 。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法叫 法;
(3)设计实验(1)对应的假设是 ;
实验(1)得出的结论是 。
(4)由实验(2)和实验(3)得出的结论是 ;
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液的离子方程式:
。
取适量固体混合物于烧杯中,加入蒸馏水搅拌,混合物完全溶解,得到无色透明溶液A,同时闻到有轻微的刺激性气味。用胶头滴管取少量溶液A于试管中,再滴加稀硝酸,溶液中有无色气泡产生;继续滴加过量稀硝酸至溶液中不再产生气泡,得到无色透明溶液B。
(1)用___________(填实验用品名称)取固体混合物于烧杯中。
(2)上述实验可以得到的初步结论是__________________________________。
19.(12分)已知某白色混合粉末中含有CuSO4、K2SO4、NH4HCO3、NH4Cl、NaCl五种物质中的两种,且物质的量之比为 1:1。请完成下述探究该混合物组成的实验。
限选择的仪器、用品和试剂:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;红色石蕊试纸、淀粉KI试纸;1mol/L硫酸、1mol/L硝酸、2mol/L盐酸、2mol/LnaOH溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水。
18、时钟反应或振荡反应提供了迷人课堂演示实验,也是一个活跃的研究领域。测定含I-浓度很小的碘化物溶液时,利用振荡反应进行化学放大,以求出原溶液中碘离子的浓度。主要步骤如是:
①在中性溶液中,用溴将试样中I-氧化成IO3-,将过量的溴除去。
②再加入过量的KI,在酸性条件下,使IO3-完全转化成I2。
③将②中生成的碘完全萃取后,用肼将其还原成I-,方程式为:N2H4+2I2=4I-+N2+4H+
④将生成的I-萃取到水层后用①法处理。
⑤将④得到的溶液加入适量的Ⅺ溶液,并用硫酸酸化。
⑥将⑤反应后的溶液以淀粉作指示剂,用Na2S2O3标准溶液滴定,方程式为:
2Na2S2O3+I2=Na2S4O6+2NaI经过上述放大后,溶液中I-浓度放大为原溶液中I-浓度的(设前后溶液体积相等)
A.2倍 B.4倍 C.36倍 D.6倍
17、在一含Na+的澄清溶液中,可能还存在NH4+、Fe2+、I-、Br-、CO32-、SO32-六种离子中的几种。①在原溶液中滴加足量的饱和氯水后,有气泡生成,溶液呈橙黄色;②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;③橙黄色溶液不能使淀粉溶液变蓝色。根据上述实验事实推断,下列说法不正确的是
A.溶液中一定存在Br-、CO32- B.溶液中可能存在NH4+
C.溶液中一定不存在Fe2+、I-、SO32- D.溶液可能呈酸性
16.某些烃的燃烧热(kJ/mol)如下表,下列表示正确的是AB
|
化合物 |
燃烧热 |
化合物 |
燃烧热 |
|
甲烷 |
891.0 |
正丁烷 |
2878.0 |
|
乙烷 |
1560.8 |
异丁烷 |
2869.6 |
|
丙烷 |
2221.5 |
2-甲基丁烷 |
3531.3 |
|
乙烯 |
1411.0 |
乙炔(C2H2) |
1300.0 |
A.热稳定性:正丁烷<异丁烷
B.乙烷燃烧的热化学方程式C2H6(g)+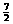 O2(g)=2CO2(g)+3H2O(l);∆H=-1560.8kJ/mol
O2(g)=2CO2(g)+3H2O(l);∆H=-1560.8kJ/mol
C.等物质的量的乙烯和乙炔(C2H2)完全燃烧,乙烯放出的热量多,故用氧烯焰来切割或焊接金属比氧炔焰好
D.相同质量的烃、碳的质量分数越大,燃烧放出的热量越多
15.将氨水滴加到盛有AgCl的试管中AgCl逐渐溶解,对上述过程下列叙述或解释中正确的有
A.所得溶液中c(Ag+)×c(Cl-)>Ksp(AgCl)
B.所得溶液中形成了更难电离的物质B
C.上述实验说明Cl-与NH4+间有很强的结合力
D.上述过程中NH3·H2O的电离程度增大
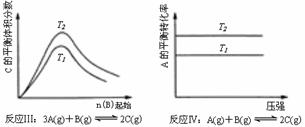
14. 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):

根据以上规律判断,下列结论正确的是
A.反应Ⅰ:△H>0,P2>P1 B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 D.反应Ⅳ:△H<0,T2>T1
13、青石棉(crocidolite)是世界卫生组织确认的一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,青石棉的化学式为:Na2Fe5Si8O22(OH)2,青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法正确的是
A、青石棉是一种易燃品且易溶于水
B、青石棉的化学组成用氧化物的形式可表示为:Na2O·3FeO ·Fe2O3·8SiO2 ·H2O
C、1mol Na2Fe5Si8O22(OH)2与足量的硝酸作用,至少需消耗6L3mol/LHNO3溶液
D、1mol Na2Fe5Si8O22(OH)2与足量氢氟酸作用,至少需消耗5.5L2mol/LHF溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com