
题目列表(包括答案和解析)
3. 已知反应:①H2(g)+ O2(g)=== H2O(g) ΔH1
②N2(g) + O2(g)
=== NO2(g) ΔH2 ③N2(g) + 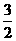 H2(g) === NH3(g) ΔH3
那么在相同温度下反应:4NH3(g)+7O2(g)===4NO2(g)+6H2O(g)的焓变为
A.4ΔH3-6ΔH1-4ΔH2 B.6ΔH1+4ΔH2-4ΔH3
C.ΔH1+ΔH2-ΔH3 D.ΔH3-ΔH1-ΔH2
H2(g) === NH3(g) ΔH3
那么在相同温度下反应:4NH3(g)+7O2(g)===4NO2(g)+6H2O(g)的焓变为
A.4ΔH3-6ΔH1-4ΔH2 B.6ΔH1+4ΔH2-4ΔH3
C.ΔH1+ΔH2-ΔH3 D.ΔH3-ΔH1-ΔH2
2. 下列说法正确的是 A.放热反应都是自发的,吸热反应都是非自发的 B.电解池的反应属于自发过程 C.反应能否自发进行与温度无关 D.熵增加且放热的反应一定是自发反应
1. 常温下,下列变化过程不是自发的是 A.石灰石的分解 B.原电池产生电流 C.氯化铵晶体与消石灰反应 D.铁在潮湿空气中生锈
2. 请将全部答案填到答题卷中。
可能用到的相对原子质量: H 1 C 12 O 16 Mg 24 K 39 Fe 56 Cu 64 Zn 65
第Ⅰ卷 (选择题 共66分)
在下列各题的四个选项中均只有一个是符合题目要求的。
1. 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共150分。考试时间120分钟。
26、(16分)镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用。
(1)Ni在元素周期表中的位置是 。
(2)镍易形成配合物,如:Ni(CO)4、[Ni(NH3)6] 2+ 等。写出一种与配体CO互为等电子体的阴离子 。配体NH3中N原子的杂化类型为 , 它可用作致冷剂的原因是 ____________________________。
若[Ni(NH3)6] 2+ 为正八面体构型,则[Ni(CO)2(NH3)4] 2+的结构有 种。
 (3) 镍常见化合价为+2、+3, 在水溶液中通常只以+2 价离子的形式存在。+3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应。Ni3+的电子排布式为
,NiO(OH)溶于浓盐酸的化学方程式为
(3) 镍常见化合价为+2、+3, 在水溶液中通常只以+2 价离子的形式存在。+3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应。Ni3+的电子排布式为
,NiO(OH)溶于浓盐酸的化学方程式为
_______________________________________________。
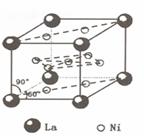
(4)镍和镧(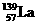 )组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x=
。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为:
)组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x=
。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为:
25.(9分)绿色有机合成是指采用无毒、无害的原料、催化剂和溶剂,选择具有高选择性、高转化率,不生产或少生产对环境有害的副产品合成。下列是BHC公司新发明的布洛芬(Ibuprofen)绿色合成方法。
试回答下列问题:
(1)反应①、③分别所属的有机反应类型是: 、 。
(2)反应①的化学方程式为: 。
(3)与布洛芬互为同分异构体的芳香族化合物中,其结构可表示为的酯类,X的结构有: 种(填数字)。
(4)某学生提议用Reppe反应一步合成布洛芬,并使原子利用率100%,已知:RCH=CH2+CO+H2ORCH(CH3)COOH,请写出用一种有机原料合成布洛芬的化学方程式:
24、(10分)

23. (12分)污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质,再用CCl4萃取络合物,把金属离子从水溶液中完全分离出来。如用双硫腙(H2Dz)-CCl4分离污水中的Cu2+时,先发生络合反应:Cu2++2 H2Dz Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
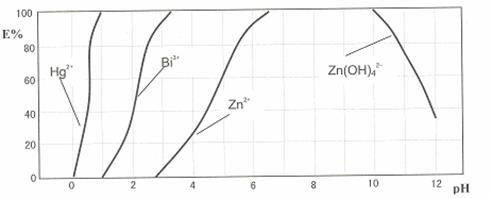
(1)写出双硫腙和Fe3+络合的离子方程式 。萃取过程中要控制适宜的酸度。如果溶液的pH过大,其后果是 。
上图是用双硫腙(H2Dz)-CCl4络合萃取某些金属离子的酸度曲线。它反映了萃取某些金属离子时适宜的pH范围。E%表示某种金属离子以络合物形式被萃取分离的百分率。某工业废水中含有Hg2+、Bi3+、Zn2+,用双硫腙(H2Dz)-CCl4络合萃取法处理废水。请根据上图回答问题:
(2)欲完全将废水中的Hg2+分离出来,须控制溶液pH=
(3)当调节pH=2时,铋(Bi)的存在形式有: ,其物质的量之比为
(4)萃取到CCl4中的Zn(HDz)2分液后,加入足量的NaOH溶液,充分振荡后,锌又转到水溶液中。写出反应的离子方程式 。
22、(8分)通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
⑴目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对环境的积极意义在于 。
⑵最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
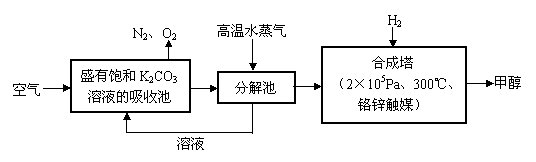
①分解池中反应的化学方程式为 。
②在合成塔中,若有4.4kg CO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程式 。
⑶李明同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp)分别为4.96×10-9、2.58×10-9。李明应该选用的试剂是 ,实验时测定的数据除空气的体积外,还需要测定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com