
题目列表(包括答案和解析)
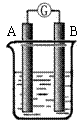
23. (8分)某研究性学习小组欲探究原电池的形成条件,按右图所示装置进行实验并得到下表实验结果:
|
实验 序号 |
A |
B |
烧杯中的液体 |
 灵敏电流计 灵敏电流计指针是否偏转 |
|
1 |
Zn |
Zn |
乙醇 |
无 |
|
2 |
Zn |
Cu |
稀硫酸 |
有 |
|
3 |
Zn |
Zn |
稀硫酸 |
无 |
|
4 |
Zn |
Cu |
苯 |
无 |
|
5 |
Cu |
C |
氯化钠溶液 |
有 |
|
6 |
Mg |
Al |
氢氧化钠溶液 |
有 |
分析上述数据,回答下列问题:
(1)实验2中电流由 极流向 极(填“A”或“B”)
(2)实验6中电子由B极流向A极 ,表明负极是 电极(填“镁”或“铝”)
(3)实验5 表明
A.铜在潮湿空气中不会被腐蚀 B.铜的腐蚀是自发进行的
C.杂质(如C、NaCl等)存在会加快铜的腐蚀速率
D.铜与铁一样,既能发生吸氧腐蚀,也能发生析氢腐蚀,
(4)分析上表有关信息,下列说法不正确的是
A.相对活泼的金属一定做负极 B.失去电子的电极是负极
C.烧杯中的液体,必须是电解质溶液
D.浸入同一电解质溶液中的两个电极,是活泼性不同的二种金属(或其中一种非金属)
22. 下列叙述正确的是 A.90℃时,纯水的pH=6.2,说明加热可导致水呈酸性 B.25℃时,pH=3的醋酸溶液稀释至10倍后pH=4 C.25℃时,0.2mol/L的盐酸与等体积水混合后pH=1 D.含有H+离子的溶液一定呈酸性
第Ⅱ卷 (非选择题 共84分)
21.
下列溶液一定呈中性的是
A.pH=7的溶液 B.c (H+)=1.0×10-7 mol/L的溶液
C.c (H+)=c
(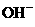 )
D.pH=3的酸与pH=11的碱等体积混合后的溶液
)
D.pH=3的酸与pH=11的碱等体积混合后的溶液
20.
在一定温度下,将CO和水蒸气各1mol置于密闭容器中反应:CO+H2O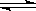 CO2+H2,达到平衡后测得CO2为0.6mol,再通入0.5mol水蒸气,达到新的平衡后CO2的物质的量可能是
A.0.6mol B.0.8mol C.1.0mol D.1.5mol
CO2+H2,达到平衡后测得CO2为0.6mol,再通入0.5mol水蒸气,达到新的平衡后CO2的物质的量可能是
A.0.6mol B.0.8mol C.1.0mol D.1.5mol
19.
 pH=2的X、Y、Z三种酸溶液各1 mL,分别加水稀释到1000 mL,其pH与溶液体积(V)的关系如下图所示,下列说法中正确的是
A.三种酸溶液的浓度:c(Z)>c(Y)>c(X)
B.三种酸中只有Z是弱酸
C.pH=2时,X、Y、Z都是稀溶液
D.稀释后三种酸中c(H+):X>Y>Z
pH=2的X、Y、Z三种酸溶液各1 mL,分别加水稀释到1000 mL,其pH与溶液体积(V)的关系如下图所示,下列说法中正确的是
A.三种酸溶液的浓度:c(Z)>c(Y)>c(X)
B.三种酸中只有Z是弱酸
C.pH=2时,X、Y、Z都是稀溶液
D.稀释后三种酸中c(H+):X>Y>Z
18. 现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是 A.加入10mL的水进行稀释 B.加水稀释成100mL C.加入10mL 0.01mol·L-1的NaOH溶液 D.加入10mL 0.01mol·L-1的HCl溶液
17. 常温时,将两种溶液等体积混合,其中溶液pH一定或可能大于7的情况是 ①pH=2盐酸和pH=12 NaOH溶液 ②pH=2醋酸和pH=12 NaOH溶液 ③pH=2盐酸和pH=12氨水 ④pH=2某酸和pH=12 NaOH溶液 ⑤pH=2盐酸和pH=12某碱溶液 ⑥pH=2硫酸和pH=12 NaOH溶液 ⑦pH=2盐酸和pH=12 Ba(OH)2溶液 ⑧pH=2硫酸和pH=12 Ba(OH)2溶液 A.③⑤ B.②④ C.⑤⑦ D.④⑤
16. 下列各组离子一定能大量共存的是 A.在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- B.在使酚酞变红的溶液中:Na+、K+、AlO2-、CO32- C.在水电离产生的c(OH-)=1×10-14mol·L-1的溶液中:NH4+、Al3+、SO42-、NO3- D.在pH试纸变深红色的溶液中:K+、Fe2+、Cl-、NO3-
15. 将等质量的锌(wg)分别投入VL,pH=3的盐酸和醋酸中,结果发现一种溶液中Zn有剩余,有关叙述正确的是 A.0.0325 V≤W<0.065V B.产生H2的量醋酸多于盐酸 C.平均反应速率盐酸大于醋酸 D.w≤0.0325 V
14.
在一个1L的密闭容器中,加入2molA和1molB,发生下述反应:
2A(g)+B(g)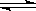 3C(g)+D(s),
达到平衡时,C的浓度为1.2mol/L。若维持容器的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2mol/L,则D的起始物质的量应满足的条件是
A.大于零即可 B.大于0.6mol C.大于或等于1mol D.任意值
3C(g)+D(s),
达到平衡时,C的浓度为1.2mol/L。若维持容器的体积和温度不变,反应从逆反应开始,按不同配比作为起始物质,达到平衡时,C的浓度仍是1.2mol/L,则D的起始物质的量应满足的条件是
A.大于零即可 B.大于0.6mol C.大于或等于1mol D.任意值
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com