
题目列表(包括答案和解析)
7. 在一定条件下,反应CO+NO2  CO2+NO 达到平衡后,降低温度,混合气体的颜色变浅。下列判断正确的是( )
CO2+NO 达到平衡后,降低温度,混合气体的颜色变浅。下列判断正确的是( )
A. 正反应为吸热反应 B. 正反应为放热反应
C. CO的浓度增大 D. 物质的浓度不变
6. 一定温度下,可逆反应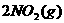

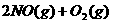 在体积固定的密闭容器
在体积固定的密闭容器
中反应,达到平衡状态的标志是( )
① 单位时间内生成n molO2,同时生成2n molNO2
② 单位时间内生成n molO2,同时生成2n molNO
③ 用NO2、NO、O2的物质的量浓度变化表示的反应速率之比为2:2:1
④ 混合气体的压强不再改变
⑤ 混合气体的颜色不再改变
⑥ 混合气体的平均相对分子质量不再改变
A. ①④⑤⑥ B. ①②③⑤ C. ②③④⑥ D. 以上全部
5. 在稀硝酸中,能大量共存的离子组是( )
A. Ag+ Cl- B. NH4+ Cl- C. I- Na+ D. CO32- K+
4. 下列操作不能用于检验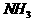 的是( )
的是( )
A. 气体使湿润的酚酞试纸变红
B. 气体能使湿润的红色石蕊试纸变蓝
C. 气体与浓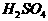 生成铵盐
生成铵盐
D. 气体与浓盐酸产生铵盐
3. 对已达化学平衡的下列反应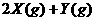

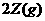 减小压强时,对反应产生
减小压强时,对反应产生
的影响是( )
A. 逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B. 逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C. 正、逆反应速率都减小,平衡向逆反应方向移动
D. 正、逆反应速率都增大,平衡向正反应方向移动
2. 把镁带投入盛有稀HCl的容器里,产生H2的速率与下列因素:① 盐酸浓度,② 温
度,③ 镁带的表面积,④溶液的氯离子浓度,有关系的是( )
A. ①② B. ③ C. ①②③ D. ①②③④
1. 在N2+3H2 2NH3的反应中,经一段时间后,NH3的物质的量浓度增加了0.6mol/ L,在此时间内用H2物质的量浓度表示的平均速率为0.45mol/(L·s),则反应所经过的时间为( )
2NH3的反应中,经一段时间后,NH3的物质的量浓度增加了0.6mol/ L,在此时间内用H2物质的量浓度表示的平均速率为0.45mol/(L·s),则反应所经过的时间为( )
A. 0.2s B. 1.0s C. 1.5s D. 2.0s
32(7分).有一硫酸和硝酸的混合溶液,取出20mL,加入足量BaCl2溶液,经过滤、洗涤、烘干后得沉淀9.32g;滤液与4mol/L的苛性钠溶液35mL恰好完全中和。试求:
⑴.原混合溶液中硫酸和硝酸的物质的量浓度。
⑵.另取20mL原溶液,加入3.2g铜粉共热,生成气体一氧化氮的体积。(标准状况下)。
30(3分).现只有酚酞试液、试设计鉴别盐酸、氢氧化钠、硫酸钠三瓶溶液的实验方案:
。
31.(8分)氨(NH3)是重要的含氮化合物。1774年该气体由英国普里斯特里利用熟石灰和氯化铵加热反应制成。
(1)写出实验室制取氨气的化学方程式 ;
(2)为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置:
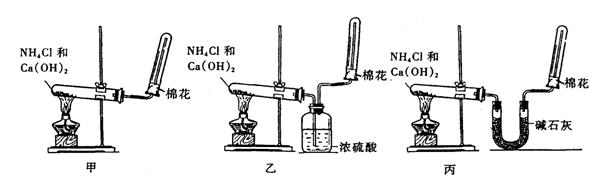
实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”) ;
(3)如何检验氨气是否收集满(简述操作方法、现象和结论) ;
(4)该实验装置与实验室制备 气的装置相同.;
28(8分).右图是某元素及其重要化合物的相互转化关系图(生成物中不含该元素的物质均已略去),图中A是单质,D在常温下呈气态,E可用作化肥,也可用来作炸药。
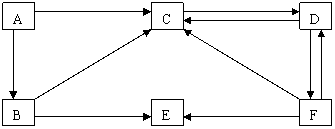
(1)写出A的电子式 ;B分子的结构呈 ;
(2)写出下列变化的化学方程式:
B→C:____________________________________________________________;
F→C:____________________________________________________________。
29(8分).有一无色透明的溶液做如下实验:
(1)取少量溶液滴加盐酸酸化的BaCl2溶液,有白色沉淀生成。
(2)另取部分溶液加入Na2O2,有无色无味气体放出且有白色沉淀生成,加入Na2O2的量与生成沉淀的量的关系如图所示:
试问:
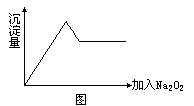
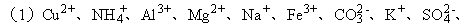 等离子中一定存在的离子是
;可能存在的离子是
;一定不存在的离子是
。
等离子中一定存在的离子是
;可能存在的离子是
;一定不存在的离子是
。
(2)上述溶液至少由 等物质混合成。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com