
题目列表(包括答案和解析)
8.酸根离子RO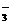 所含电子数比NO
所含电子数比NO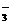 的电子数多10,则下列说法中正确的是 ( )
的电子数多10,则下列说法中正确的是 ( )
A.R原子的电子层数与N原子电子层数相同
B.RO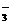 中R的化合价与NO
中R的化合价与NO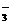 中的N的化合价相同
中的N的化合价相同
C.RO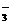 中的R元素既能被还原,也能被氧化
中的R元素既能被还原,也能被氧化
D.R与N为同族元素
7.曾报导合成和分离了含高能量的正离子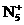 的化合物N5AsF6,下列描述中错误的是
( )
的化合物N5AsF6,下列描述中错误的是
( )
A.N5+共有34个核外电子
B.N5+中氮氮原子间以共用电子对结合
C.化合物N5AsF6中As化合价为+1
D.化合物N5AsF6中F化合价为-1
6.不同浓度的HNO3分别与一定量的锌粉完全反应,还原产物分别为NO2、NO和NH4NO3,若反应的锌物质的量相等时,参加反应的硝酸物质的量之比是 ( )
A.2∶4∶5 B.1∶2∶5 C.1∶2∶2 D.24∶16∶15
5.现有10mLNO和NO2混合气体,其平均相对分子量为36.4,通入一定量的O2后,还是10mLNO和NO2混合气体,但平均相对分子量为39.6,通入O2的体积是 ( )
A.1mL B.3mL C.5mL D.10mL
4.FeS2与HNO3反应后的氧化产物为Fe(NO3)3和H2SO4,若反应中FeS2与HNO3的物质的量之比为1∶8,则HNO3的还原产物为 ( )
A.NO2 B.NO C.N2O D.N2O3
3.向1L 0.5mol/L的H2SO4溶液中加入10.1gKNO3和12.8gCu充分反应后产生的气体在标准状况下的体积为 ( )
A.2.24L B.3.36L C.4.48L D.5.60L
2.砒霜中毒事件时有发生,砒霜的主要成分是三氧化二砷(As2O3),医生通常给砒霜中毒患者服用一定剂量的氧化剂解毒。下列有关叙述正确的 ( )
A.砷元素在化合物中的常见价态有+3、+5、+7 B.砷酸(H3AsO4)的酸性强于磷酸
C.砷化氢(AsH3)比NH3稳定 D.砷的+3价化合物的毒性强于+5价化合物
1.机床的废切液中含有2%~5%的亚硝酸钠,直接排放会造成环境污染,为使其能除去NO2-‑,并且不引起第二次污染出现,应选用的试剂是 ( )
A.HNO3 B.NH4Cl C.FeSO4 D.浓H2SO4
关键词: 电离平衡 高中化学 同步课堂
|
化学平衡图象题总汇 |
|||||||||||||||||||||
|
文/张存学 |
|||||||||||||||||||||
图象题是化学平衡中的常见题型,是勒沙特列原理等化学平衡知识在直角坐标系中的直观反映。同时,它又是化学平衡的重点、难点,学生的疑惑点、失分点。怎样解决有关图象问题呢?下面将举例讨论。
一、图象题的一般解题思路
这类题目是讨论自变量x(如时间、温度、压强等)与函数值y(如物质的量、浓度、质量分数、转化率)之间的定量或定性关系,因此,要运用数学方法解决此类题目。
1.分析纵横坐标及曲线表示的意义。
2.分析曲线的变化趋势与纵横坐标的关系。
3.分析特殊点(起点、拐点、终点)及其含义。
4.有两个以上变量时,分别讨论两个变量的关系,此时确定其他量为恒量。
二、图象题的类型
1.物质的量(或浓度)-时间图象
例1.某温度下,在体积为5L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图1所示,则该反应的化学方程式为_________,2s内用A的浓度变化和用B的浓度变化表示的平均反应速率分别为_________、_________。
[分析]这类题目是讨论同一时间段内各物质的变化量的比例关系,且要注意物质的量减少的为反应物,物质的量增多的为生成物。又因物质的量都不变时,反应物、生成物共存,故方程式要用“
[分析] 这类题目是讨论速率受外界条件影响而变化的图象。因速率随时间延长先升高后降低,故速率要受反应过程中物质的浓度、温度(或压强)两种因素变化的影响。
[答案]反应是放热反应,温度升高使化学反应速率提高;盐酸物质的量浓度变小使化学反应速率降低。
例3.某温度下,在密闭容器里SO2、O2、SO3三种气态物质建立化学平衡后,改变条件,对反应2SO2+O2
①加催化剂对速率影响的图象是( )。
②升温对速率影响的图象是( )。
③增大反应容器体积对速率影响的图象是( )。
④增大O2的浓度对速率影响的图象是( )。
[分析]这类图象是讨论外界条件对化学平衡的影响。解决这类题目的关键是分析改变条件的瞬间,正、逆反应速率的变化及变化幅度。
[答案]①C
②A ③D ④B
3.速率-压强(或温度)图象
例4.符合图象4的反应为( )。
A.N2O3(g)
[分析]此类图象中曲线的意义是外界条件(如温度、压强等)对正、逆反应速率影响的变化趋势及变化幅度。
答案 B
4.转化率(或质量分数等)-压强、温度图象
例5.有一化学平衡mA(g)+nB(g)
A.正反应吸热,m+n>p+q
B.正反应吸热,m+n<p+q
C.正反应放热,m+n>p+q
D.正反应放热,m+n<p+q
[分析]解决这类图象题目,采用“定一论二”,即把自变量(温度、压强)之一定为恒量,讨论另外两个变量的关系。
答案 A
例6.mA(s)+nB(g)
[分析]这类题目中曲线是表示“平衡”时,质量分数与压强(或温度)变化关系曲线。X、Y点则未达平衡状态,反应要向“趋向于平衡状态方向”进行,以此判断某点v正、v逆的大小关系。比较X、Y两点的速率快慢则依据压强的高低(或温度的高低)。
答案 A、C
例7.图7表示mA(g)+nB(g)
A.m+n>p+q Q>0
B.m+n>p+q Q<0
C.m+n<p+q Q>0
D.m+n<p+q Q<0
[分析]图7中,生成物的质量分数受同种外界条件的影响呈现两种变化趋势,则这两种趋势一定是平衡前、后的两种情况,故最高点时刚好建立平衡,其后,才为外界条件对平衡的影响。
答案 C
5.质量分数-时间图象
例8.对于可逆反应mA(g)+nB(s)
答案
A、C
以上是常见的几种平衡图象及一般解题思路,具体问题要注意综合、灵活地运用。
例9.反应2X(g)+Y(g)
|
27.(本题9分)饱和一元羧酸X和饱和一元醇Y可形成A、B两种酯。试回答:
①它们的混合物中碳元素的质量分数为48.65%时,氧元素的质量分数为_____________;
②等物质的量的A、B混合物中取1 mol ,完全燃烧时消耗3.5 mol氧气,且A、B都能发生银镜反应,A的式量小于B,则A、B的结构简式为A___________________
B________________________;
③取50 mL物质的量浓度为1.2 mol/L的X溶液与足量的银氨溶液充分反应后,可得沉淀物多少克?
|
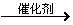 2CH3CHO,
2CH3CHO,
CH=CH+H2O 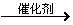 CH3CHO。22.⑴相等 ⑵甲醛,石炭酸
⑶C3H8O,能
CH3CHO。22.⑴相等 ⑵甲醛,石炭酸
⑶C3H8O,能
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com