
题目列表(包括答案和解析)
3. 区别手织品与棉织品最简单的方法是
A. 放入稀硫酸中,加热水解
B. 放入氢氧化钠溶液中,加热水解
C. 滴上浓硝酸,看是否变黄
D. 取一丝灼烧,看是否“起球”,是否的烧焦羽毛的气味
2. 新产品“不粘锅”受到广大群众的欢迎,其生产工艺十分简单:在金属锅的内壁上涂一层聚四氟乙烯。下列说法中正确的是
A.聚四氟乙烯的结构简式是 F2C==CF2
B. 聚四氟乙烯中含碳, 所以在加热时能够燃烧生成二氧化碳
C.由于C-C键和F-C键很牢固,因而聚四氟乙烯的性质稳定,在使用时不会污染食物
D.聚四氟乙烯中不能与常见的氧化剂接触, 防止被氧化
1. 工业酒精和用粮食发酵产生的酒精的成份不完全相同。严禁用工业酒精勾兑食用酒,否则会使人双目失明甚至死亡。工业酒精中的有毒成份是
A. CH3OH B. CH3CH2OH C. CH3COOC2H5 D. CH3COOCH3
35.(8分)向100 mL某二价金属M的氢氧化物澄清溶液中加入过量的 NaHCO3溶液,生成了MCO3沉淀,过滤,将沉淀置于足量的盐酸溶液中,在标准状况下收集到4.48L气体。将滤液加水稀释至 250 mL,取出 25 mL恰好与 20 mL盐酸完全反应,在标准状况下收集到1.12L气体。
(1)M的氢氧化物澄清溶液与NaHCO3溶液反应的化学方程式为:
___ __。
(2)要计算金属M的原子量,你认为还必须提供下列哪项数据(填写供选项字母序号)____。
(A)M的氢氧化物溶液的物质的量浓度(设为2mol·L-1)
(B)M的碳酸盐的质量(设为39.4 g)
(C)与M的碳酸盐反应的盐酸的物质的量浓度(设为 0.1mol·L-1)
(D)题设条件充足,不需要补充数据。
(3)根据你的选择,试计算金属M的原子量和加入的NaHCO3溶液中所含的NaHCO3的质量。
1999-2000学年度第二学期期末高二化学试卷
34、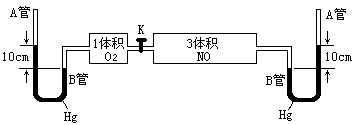 (6分)如图所示,打开两个容器间的活塞K,使两种气体混合,充分反应,达到平衡状态时(温度不变),A管中汞液面比B管中汞液面高7.1cm,(反应开始时高10cm),设此温度
(6分)如图所示,打开两个容器间的活塞K,使两种气体混合,充分反应,达到平衡状态时(温度不变),A管中汞液面比B管中汞液面高7.1cm,(反应开始时高10cm),设此温度
产物为气态,汞蒸汽压忽
略不记,体系容积为定值。
求NO2转化为N2O4的转
化率。
33、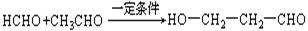 (9分)已知:①乙醛甲基上的氢原子是α氢原子,活性较大,可以与甲醛中的醛基发生加成反应,如:
(9分)已知:①乙醛甲基上的氢原子是α氢原子,活性较大,可以与甲醛中的醛基发生加成反应,如:
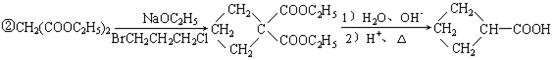
现由乙烯和丙二酸等物质合成I,合成路线如下:
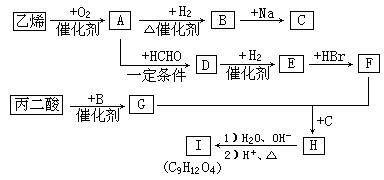
请回答下列问题:
(1)写出下列物质的结构简式:
E 、H
I ;
(2)写出A→D的化学方程式:(有机物写结构简式):
。
32、(8分)某α-氨基酸,分子量不超过200,经分析可知,该氨基酸含C、H、O、N四种元素,其中氮元素的质量分数为8.5%,氧的质量分数为19.4%。
(1)该氨基酸的分子中有 个-NH2, 个-COOH。
(2)该氨基酸分子量(取整数值)为 。
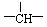 (3)若氨基酸分子结构中无甲基(-CH3),有和苯环,写出其结构简式
。
(3)若氨基酸分子结构中无甲基(-CH3),有和苯环,写出其结构简式
。
(4)另有一种有机物A是上述氨基酸的同分异构体,A分子中也含有苯环,但不含-NH2和-COOH,且苯环上的一卤代物只有一种,则A的结构简式可能
为: 、 。
31.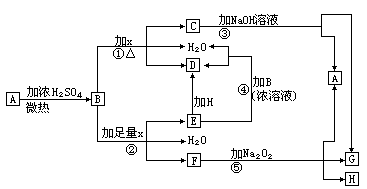 (9分)物质A-H有下图所示转化关系(部分反应物、生成物没有列出)。其中,B的浓溶液与单质X在加热时才能发生反应①,B的稀溶液与足量X发生反应②,向C溶液中滴入KSCN溶液呈红色。
(9分)物质A-H有下图所示转化关系(部分反应物、生成物没有列出)。其中,B的浓溶液与单质X在加热时才能发生反应①,B的稀溶液与足量X发生反应②,向C溶液中滴入KSCN溶液呈红色。
试填写下列空白:
(1) 晶体A是(化学式)________________________。
(2)反应②的离子方程式:______________________。
(3)根据图示信息判断,足量B的浓溶液与单质X共热时能否产生E,说明理由(写出化学方程式回答):____________________。
(4)在反应⑤中,若生成物G与H的物质的量之比为4∶1,写出F溶液与Na2O2反应的化学方程式:_______________________。
30.(6分)已知25℃时0.1mol·L-1醋酸溶液的pH约为3。向其中加入少量醋酸钠晶体,待晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了[OH-],因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使[H+]减小,因此溶液的pH增大。
你认为上述两种解释中___ __(“甲”或“乙” )正确。
(1) 为了验证上述哪种解释正确,继续做如下实验:向0.1mol·L-1的醋酸溶液中加入少量下列物质_____。(填写编号),然后测定溶液的pH。
(A)固体CH3COOK (B)固体CH3COONH4
(C)气体NH3 (D)固体NaHCO3
(2)若____(填“甲”或“乙” )的解释正确,溶液的pH应____(填“增大”、“减小”或“不变” )。
(已知:25℃时,0.1mol·L-1氨水的电离度为1.3%,0.1mol·L-1醋酸的电离度为1.3%)
29、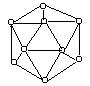 (4分)已知晶体硼的基本结构单元是由硼原子组成的正二十面体(如图所示),其中有二十个等边三角形的面和一定数目的顶角,每个顶点各有一个硼原子。通过观察图形及推算得出此基本单元是由 个硼原子构成。其中B-B键的键角为
。
(4分)已知晶体硼的基本结构单元是由硼原子组成的正二十面体(如图所示),其中有二十个等边三角形的面和一定数目的顶角,每个顶点各有一个硼原子。通过观察图形及推算得出此基本单元是由 个硼原子构成。其中B-B键的键角为
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com