
题目列表(包括答案和解析)
2.答卷前将密封线内的项目填写清楚。
18. 将60 mL甲烷和乙烷的混合气体与210 mL氧气混合,点火燃烧,将反应后的混合物通过浓硫酸充分吸收后,得剩余气体130 mL(气体体积均在同温同压下测定),则下列叙述中正确的是
A.所得130 mL剩余气体中是CO、CO2的混合物
B.所得130 mL剩余气体的平均相对分子质量是30
C.60 mL混合气体含甲烷为20 mL
D.根据题给条件无法求出60 mL混合气体中甲烷或乙烷的体积
徐州市2005--2006学年度年第一学期期末考试
高二化学试题(必修加选修)
第二卷 (非选择题 共76分)
l.用钢笔或圆珠笔(除题目有特殊规定外)直接答在试卷上。
17.T °C时气体A与气体B在某容器中反应生成气体C和固体D,每1 mol A与足量B完全反应时生成1 mol D,反应过程中A、B、C浓度变化如图①所示。若保持其他条件不变,温度分别为T1和T2时,B的体积百分含量与时间的关系如图②所示。
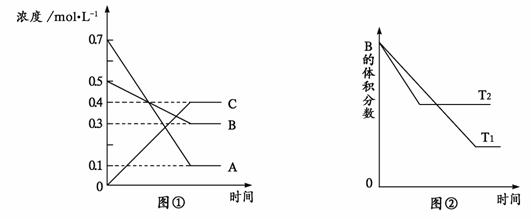
则下列结论正确的是
A.该反应的化学方程式是 A+3B 2C+D
2C+D
B.T°C时,保持容器体积不变,若向上述平衡体系中加入0.2 mol C,则重新达平衡时B的浓度小于0.3 mol/L
C.其它条件不变,升高温度时,正、逆反应速率均增大,且A的转化率减小
D.相同时间内,消耗0.3 mol/L A时,生成了0.1 mol/L B,则反应达到平衡
16.下列各图象中,横坐标为向某溶液中加(通)入某反应物的物质的量,纵坐标为沉淀物的量,则下列叙述中错误的是
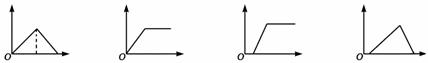
A B C D
A. 向氯化铝溶液中加入过量的氨水,其图像是B
B. 向饱和石灰水中通入过量的CO2气体,其图像是A
C. 向MgCl2、AlCl3的混合液中逐滴加入NaOH溶液至过量,其图像是D
D. 向含少量NaOH的偏铝酸钠溶液中通入过量的CO2气体,或向其中逐滴加入稀盐酸,其图像都是C
15.某金属元素M的常见化合价有+4和+6,其与氮、氧元素组成的化合物MO2(NO3)2受热可发生的分解反应为:
MO2(NO3)2-- MXOY + NO2↑+ O2↑
在600 K 时,将气体产物收集于试管中并倒扣于水中,气体全部被吸收、水充满试管。则生成的M的氧化物的化学式是
A.MO3 B.MO2 C.MO2·2MO3 D.2MO2·MO3
14. 设NA表示阿伏加德罗常数的值,下列叙述中正确的是
A. 1 L 1 mol·L-1的盐酸溶液中,所含氯化氢分子数为NA
B. 标准状况下,11.2 L四氯化碳所含分子数为0.5NA
C. 1 mol CnH2n+2含有(3n+1)NA个共价键
D. 其他条件不变时,将1 mol NO2气体进行加压,加压后气体的分子数将少于NA个
13.下列各组离子一定能大量共存的是
A.在含大量Fe3+的溶液中:NH4+、Mg2+、Cl-、SCN-
B.在强碱溶液中:Na+、K+、AlO2-、CO32-
C.在c (H+) =10-13 mol/L 的溶液中:NH4+、Al3+、SO42-、NO3-
D.pH=13的溶液中:Cu2+ 、K+、NO-3、Cl-
12.2004年美国圣路易斯大学科学家研制了一种新型的 乙醇电池(DEFC),它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 = 2CO2 +3H2O。电池示意图如下图。
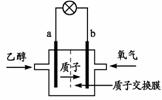
下列说法不正确的是
A. a极为电池的负极
B. 电池工作时电流由b极沿导线经灯泡再到a极
C. 电池正极的电极反应为:4H+ +O2 +4e- = 2H2O
D. 若有1 mol乙醇被氧化,则转移的电子为6 mol
11.关于小苏打水溶液的表述正确的是
A.存在的电离只有:HCO3-  H+ +
CO32-,H2O
H+ +
CO32-,H2O  H+ +
OH-
H+ +
OH-
B.HCO3-的电离程度小于HCO3-的水解程度
C.c (Na+) + c (H+)= c (HCO3-)+ c (CO32-)+ c (OH-)
D.c (Na+) = c (HCO3-)+ c (CO32-)+ c (H2CO3)
10. 下列用来表示物质变化的反应式中,正确的是
A.钢铁腐蚀时可能发生的正极反应:2H2O + O2 + 4e- = 4OH-
B.常温下,NaHCO3溶液显碱性:HCO3- + H2O 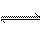 CO32-+ H3O+
CO32-+ H3O+
C.氢氧化镁与稀硫酸反应: H+ + OH- = H2O
D.硫酸亚铁酸性溶液中加入过氧化氢:2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com