
题目列表(包括答案和解析)
21.将10g铁粉置于40mlHNO3溶液中,微热,反应过程随着HNO3
浓度的降低生成气体的颜色由红棕色变为无色.充分反应后,
共收集1792mlNO、NO2的混合气体,溶液中还残留4.4g固体.
(1)求该反应中被还原和未被还原的HNO3的物质的量之比.
(2)求原HNO3溶液物质的量浓度.
20.氨(NH3)是重要的含氮化合物。1774年该气体由英国普里斯特里利用熟石灰和氯化铵加热反应制成。
(1)写出实验室制取氨气的化学方程式 ;
(2)为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置:
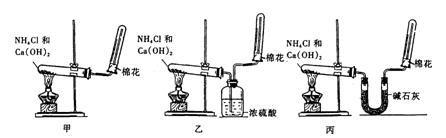
实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”) ;
(3)如何检验氨气是否收集满(简述操作方法、现象和结论)
;
 (4)该实验装置与实验室制备 气的装置相同.;
(4)该实验装置与实验室制备 气的装置相同.;
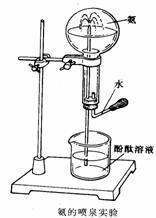
(5)如右图在圆底烧瓶里收集干燥的氨气。挤压胶头滴管中的
少量水,使它射入烧瓶中,接着你会观察到的现象是
,该现象说明氨气具有
的性质是 , ;
(6)有同学用氨的喷泉实验装置做喷泉实验,但实验失败,请
分析实验失败的可能原因
(写出任何一个合理答案即可)。
19.恒温下,将amolN2与bmolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g) + 3H2 (g) 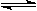 2NH3(g)
2NH3(g)
(1)若反应达平衡前某时刻t时,n(N2)=13mol,n (NH3)=6mol,则a=________mol。
(2)反应达平衡时,若混合气体的体积为716.8L(已换算为标况下),其中NH3的含量(体积分数)为25%。则平衡时NH3的物质的量为__________________。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同) n(起始):n(平衡)= ;原混合气体中,a:b=
(4)达到平衡时,N2和H2的转化率之比,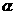 (N2) :
(N2) : 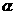 (H2) =
(H2) =
18.向体积为2L的固定密闭容器中通入3molX气体,在一定温度下发生如下反应:2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min后反应达到平衡,此时测得容器内的庄强为起始时的1.2倍,则用Y的物质的量浓度变化表示的速率为 mol/L·min。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲v(X)=3. 5mol/L·min; 乙v(Y)=2mol/L·min; 丙v(Z)=4.5mol/L·min; 丁v(X)=0. 075mol/L·s 。若其它条件相同,温度不同,则温度由高到低的顺序是(填序号)
(3)若向达到(1)的平衡体系中充入氮气,则平衡向 (填"左"或"右"或"不移动");若向达到(1)的平衡体系中移走部分混合气体,则平衡向 (填" 左 " 或 " 右 " 或 " 不 移动")。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5molX气体,则平衡后X的转化率⑷与⑴的平衡中的X的转化率相比较
A.无法确定 B.⑷一定大于⑴
C.⑷一定等于⑴ D.⑷一定小于⑴
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,则a、b、C应该满足的关系为
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则C的取值范围应该为
17.在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) CO2(g)十H2
(g);△H<0.
CO和H2O浓度变化如下图,则 0-4min的平均反应速率v(CO)=______ mol/(L·min)
CO2(g)十H2
(g);△H<0.
CO和H2O浓度变化如下图,则 0-4min的平均反应速率v(CO)=______ mol/(L·min)
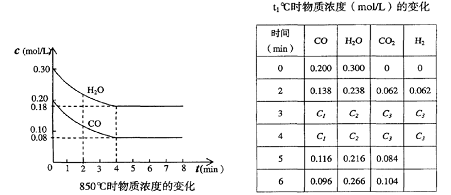
t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min-4min之间反应处于_________状态;C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min-5min问,平衡向逆方向移动,可能的原因是________(单选),
表中5min-6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
16.已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
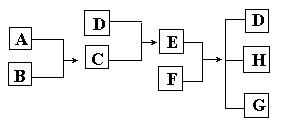
(1)D的化学式(分子式)是_____________,E的化学式(分子式)是_____________。
(2)A和B反应生成C的化学方程式是______________________________。
(3)E和F反应生成D、H和G的化学方程式是___________________________________。
15.在2L密闭容器中加入或通入一定量A、B、C三种物质,在一定条件下发生反应(如图1),3min后给体系加热,气体C的体积分数Ψ(C)和混合气体的平均相对分子质量M均随温度分别发生了图示变化(如图2、图3)。下列有关说法不正确的是 ( )
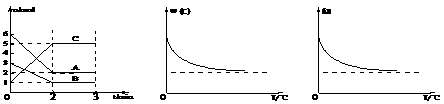
图1 图2 图3
A.前2min中C的平均反应速率为1mol/L·min
B.该反应的化学方程式为:2A+B 2C
2C
C.正反应是放热反应
D.A、B一定均为气态
|
14.某温度下,在密闭容器中发生如下反应:2M(g)+N(g) 2E(g),若开始时只充入2mol
E,达到平衡时,混合气体的压强比起始增大了20%;若开始时只充入了3mol M和1mol N的混合气体,达到平衡时M的转化率为 ( )
A.<60% B.=40% C.<40% D.>60%
13.密闭容器中,反应xA(g)+yB(g) zC(g)达到平衡后测得A气体的浓度为0.5mol•L-1。保持温度不变,将密闭容器容积增加一倍,当达到新的平衡时,测得A的浓度为0.3mol•L-1,则下列叙述中正确的是 ( )
zC(g)达到平衡后测得A气体的浓度为0.5mol•L-1。保持温度不变,将密闭容器容积增加一倍,当达到新的平衡时,测得A的浓度为0.3mol•L-1,则下列叙述中正确的是 ( )
A.平衡向正反应方向移动 B.x+y>z
C.物质C的体积分数增大 D.物质B的转化率增大
12.在一定温度不同压强(p1<p2=下,可逆反应2X(g)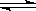 2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(
2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(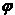 )与反应时间(t)的关系有以下图示,正确的是 ( )
)与反应时间(t)的关系有以下图示,正确的是 ( )
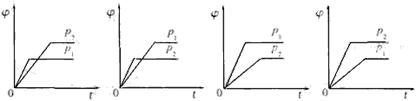
A B C D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com