
题目列表(包括答案和解析)
20.(9分)2001年9月11日,恐怖分子驾驶波音757飞机以900km/h的速度撞击纽约世贸大厦,已知波音757飞机长80m,总质量110t,其中携带航空煤油30t,煤油的燃烧值为4.62×104kJ/kg,试回答下列问题:航空煤油是石油分馏产品之一,其主要成份是分子中含碳原子个数10-15的烷烃.飞机撞击大厦时,煤油在燃烧爆炸所产生的高温条件下,有一部分迅速发生裂化,生成碳原子更少的烃,加剧了爆炸程度.
①假如煤油成份之一A的分子中含有碳原子nA个,可能裂化为B和C两种烃,其分子中分别含碳原子nB和nC个,且B为烷烃.则下列组合中正确的是________(填序号,多选或错选倒扣分).
|
|
nA |
nB |
nC |
|
a |
10 |
9 |
1 |
|
b |
11 |
6 |
5 |
|
C |
12 |
5 |
6 |
|
d |
13 |
9 |
3 |
|
e |
14 |
8 |
6 |
|
f |
15 |
11 |
4 |
②请写出上述b组所得到的烯烃中,主链上有4个碳原子的同分异构体的结构简式:
、 、 。
19.(14分)反应A(g)+B(g)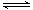 C(g)
+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)
+D(g)过程中的能量变化如图所示,回答下列问题。
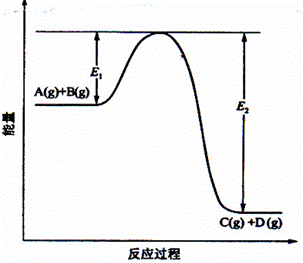
(1)该反应是____________________反应(填“吸热”“放热”);
(2)当反应达到平衡时,升高温度,A的转化率______(填“增大”“减小”“不变”),
原因是____________________________________________;
(3)反应体系中加入催化剂对反应热是否有影响?_______________,原因是_________。
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2________(填“增大”“减小、”“不变”)。
18.与水的离子积KW相似,难溶物在水中溶解部分电离出的阴阳离子浓度的乘积称为该难溶物的溶度积,用符号“Kap”表示,例如某难溶物AB在水中的溶解过程可表示为:
 AB(s)
AB(s) 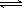 A+(aq)+ B-(aq), Kap(AB) = c(A+)c(B-);某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
A+(aq)+ B-(aq), Kap(AB) = c(A+)c(B-);某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
A.加入Na2SO4可以使溶液由a点
变到b点
B.通过蒸发可以使溶液由d点变
到c点
C.d点无BaSO4沉淀生成
D.a点对应的Kap大于c点对应
的Kap
第Ⅱ卷(非选择题 共54分)
17.在一定条件下,合成氨反应达到平衡后,混和气体中NH3的体积占25%。若反应前后条件保持不变,则反应后缩小的气体体积与原反应物体积的比值为: ( )
A. 1/5 B. 1/4 C. 1/3 D. 1/2
16. 向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(S、T、P)的气体。所得溶液中加入KSCN溶液无血红色出现,混合物中铁元素的质量分数为: ( )
A. 68.6% B. 77.8% C. 81.4% D. 无法计算
15. 某稀硝酸能与5.4g铝恰好反应,当这份酸在与铁反应时,最多消耗铁的量为: ( )
A. 0.35mol B. 0.3mol C. 0.25mol D. 0.2mol
14.一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生反应:
2SO2(g)+O2(g)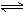 2SO3(g)达到平衡后改变下述条件,SO3气体平衡浓度不改变的是:( )
2SO3(g)达到平衡后改变下述条件,SO3气体平衡浓度不改变的是:( )
A. 保持温度和容器体积不变,充入1molSO3(g)
B. 保持温度和容器内压强不变,充入1molSO3(g)
C. 保持温度和容器内压强不变,充入1molO2(g)
D. 保持温度和容器内压强不变,充入1molAr(g)
13.一种新型燃料电池,它是用两根金属做电极插入KOH溶液中,然后向两极上分别通甲烷和氧气,其电池反应为:
X极:CH4+10OH--8e-=CO32-+7H2O Y极:4H2+2O2+8e-==8OH-
下列关于此燃料电池的有关说法中错误的是 ( )
A.通过甲烷的电极(X)为电池的负极,通过氧气的电极(Y)为电池正极
B.放电一段时间后,电解质溶液中KOH的物质的量改变
C.在标准状况下,通过5.6L氧气,完全反应后有1.0mol的电子发生转移
D.放电时,通过甲烷的一极附近的pH升高
12.实验室现有3种酸碱指示剂,其pH的变色范围如下:
甲基橙:3.1-4.4 石蕊:5.0-8.0 酚酞:8.2-10.0
用0.1000mol·L-1NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述正确的是( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
11.某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是:( )
A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量的NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入足量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com