
题目列表(包括答案和解析)
4.用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)
构成一个原电池。以下有关该原电池的叙述正确的是 ( )
①在外电路中,电流由铜电极流向银电极 ②正极反应为:Ag++e-=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A. ①② B.②③ C.②④ D.③④
3.在盛有稀硫酸的烧杯中放入用导线连接的锌片和铜片,下列叙述中正确的是 ( )
A.正极附近的SO42-离子浓度逐渐增大 B. 电子通过导线由铜片流向锌片
C.正极上有O2逸出 D. 铜片上有H2逸出
2.下列原电池的叙述中正确的是 ( )
A.构成原电池的正极和负极的材料必须是两种活泼性不同的金属
B.原电池是把化学能转变为电能的装置
C.在铅、银和盐酸构成的原电池工作时,铅板上有5.18g铅溶解,正极上就有1120mL
(标准状况)气体析出
D.原电池工作时,正极和负极上发生的都是氧化还原反应
1.一个原电池的总反应的离子方程式是Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是 ( )
|
|
A |
B |
C |
D |
|
正极 |
Zn |
Cu |
Zn |
Fe |
|
负极 |
Cu |
Zn |
Ag |
Zn |
|
电解质溶液 |
CuCl2 |
H2SO4 |
CuSO4 |
CuCl2 |
21.(6分)有一包铁粉和氧化铁粉的混合物共19.2克,恰好溶于150mL某稀H2SO4中,反应完毕后不留残渣,向溶液中滴入KSCN溶液也不显红色,反应过程中共放出3.36L标况下的H2。求:
(1)混合物中铁粉的质量?
(2)稀硫酸的物质的量浓度至少是多少?
20.(9分)有一种透明溶液,已知其中可能含有Fe3+、NH4+、Al3+、Mg2+。向该溶液中加入一种淡黄色粉末,并微热,产生有刺激性气味的混合气体,同时生成白色沉淀,当加入0.4mol淡黄色粉末时,共收集到0.3mol混合气体(假设所生成的气体全部逸出),且此时生成的沉淀量最多。再继续加入淡黄色粉末0.05mol,沉淀由0.3mol减小到0.2mol,且再加粉末时,沉淀也不再减少。由实验现象和有关数据判断:
(1)淡黄色粉末是 。
(2)原溶液中肯定没有的离子是 。
(3)原溶液中肯定有的离子是 ,其物质的量之比是 。
19.在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的是:
(填粒子的化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的是
(2)现提供以下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
请判断哪位同学的推断是正确的.并用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
|
同学正确 |
选用试剂 |
实验现象 |
|
第一种方法 |
|
|
|
第二种方法 |
|
|
(3)若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,你认为 (填“可行”或“不可行”)
理由是:
根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子是
写出在稀溴化亚铁溶液中通入足量氯气时的离子方程式:
18.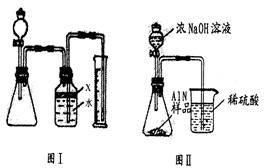 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域。某氮化铝中含有碳或氧化铝杂质,现用图Ⅰ装置来进行实验,
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域。某氮化铝中含有碳或氧化铝杂质,现用图Ⅰ装置来进行实验,
使氮化铝样品和NaOH溶液反应:
AlN+NaOH+H2O=NaAlO2+NH3↑,根据
反应中所生成氨气的体积来测定样品中
的氮化铝的质量分数,并根据实验现象
来确定杂质的成分(实验中导
管体积忽略不计)。(1)实验有关操作为:
a.往锥形瓶中放入适量的A1N样品
b.从分液漏斗往锥形瓶中加入过量的浓NaOH
c.检验装置的气密性
d.测定收集到水的体积
正确的操作顺序为 。
(2)广口瓶中的试剂x应选用
A.NaOH 溶液 B.酒精 C.植物油 D.CCl4
(3)广口瓶内的液体没有装满(上方留有少量空间),实验测得NH3的体积将
(填“偏大”、“偏小”或“不变”)。
(4)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是 。
(5)若实验中测得样品的质量为w g,氨气的体积为a mL(标况下),则样品中AIN的百分含量为 。
(6)有人改用图Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AIN的质量分数。你认为是否可行? (填“可行”或“不可行”)。原因是
,改进的方法为
17.在100mLamol/L的AlCl3溶液中加入100m Lbmol/LNaOH溶液。
(1)当b≤3a,生成Al(OH)3沉淀的物质的量为
(2)当a 、b满足 条件时,先有沉淀生成,后又有部分沉淀溶解,此时的质量为
16.铝和铁在地壳中的含量仅次于氧和硅,居于第三位和第四位,现代生活离不开它们。根据铝、铁单质及其化合物的性质和用途。回答下列问题。
(1)向灼热的铁丝喷洒水,用化学方程式表示 。
(2)氢氧化铝是几乎不溶于水的白色胶状物,但它易溶于强酸或强碱溶液,请用离子方程式表示 , 。
(3)明矾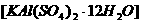 可用于净水。在明矾的水溶液中滴入紫色石蕊试液,溶液呈 色,这是因为(用离子方程式表示)
;再加热,观察到的现象是
,简述原因
。
可用于净水。在明矾的水溶液中滴入紫色石蕊试液,溶液呈 色,这是因为(用离子方程式表示)
;再加热,观察到的现象是
,简述原因
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com