
题目列表(包括答案和解析)
14.将含有KCl、CuCl2和Na2SO4三种物质的水溶液(浓度均为1mol/L)用铂电极电解,经过足够长时间后,有以下说法:① 溶液中几乎无Cl- ② 电解质溶液变为无色 ③ 最后所的溶液呈碱性 ④ K+、Na+和SO42-浓度几乎没有变化 ⑤ 电解过程根据电极产物,可明显分为三个阶段,在阴极上依次生成铜、氯气、氢气。结论正确的是 ( )
A.①②③ B.①②⑤ C.④⑤ D.①②③④⑤
13.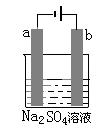 右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊试液,下列实验现象中正确的( )
右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊试液,下列实验现象中正确的( )
A.逸出气体的体积a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近出现蓝色
D.a电极附近呈蓝色,b电极附近出现红色
12.下列叙述正确的是 ( )
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
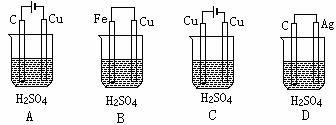
11.某同学欲完成反应:Cu+H2SO4=CuSO4+H2↑,而设计了下列四个实验装置,你认为可行的是 ( )
10.1L 0.1mol/L AgNO3溶液在以Ag作阳极,Fe作阴极的电解槽中电解,当阴极上增重2.16g时,下列判断正确的是(设电解在理想状况下进行,溶液不蒸发) ( )
A.溶液的浓度变为0.08 mol/L B.阳极上产生112 mL O2(标准状况)
C.转移的电子数是1.204×1022 D.反应中有0.02 mol的Ag+被氧化
9.下图中x、y分别是直流电源的两极,通电后发现,a极板质量增加,b极板有无色无臭气体放出,符合这一情况的是 ( )

|
|
a极板 |
b极板 |
x电极 |
电解质溶液 |
|
A |
锌 |
石墨 |
负极 |
CuSO4 |
|
B |
石墨 |
石墨 |
负极 |
NaOH |
|
C |
银 |
铁 |
正极 |
AgNO3 |
|
D |
铜 |
石墨 |
负极 |
CuCl2 |
8.蓄电池的两极分别为Pb、PbO2,电解液为H2SO4,工作时的反应为:Pb+PbO2+2H2SO4=2PbSO4+2H2O ,下列有关叙述正确的是 ( )
A.Pb为正极,被氧化 B.溶液的PH不断减小
C.SO42-只向PbO2极移动 D.电解质溶液的密度不断减小
7.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是 ( )
A.充电时阳极反应:Ni(OH)2 -e- + OH-== NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
6.据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服
务。某种氢氧燃料电池是用两根铂丝作电极插入KOH溶液中,再分别向两极通入甲烷气
体和氧气形成的原电池。该电池放电时发生的反应为CH4+2KOH+2O2=K2CO3+3H2O,
下列说法错误的是 ( )
A.通甲烷的一极为负极,通氧气的一极为正极
B.放电时,通入O2的一极附近溶液的PH升高
C.放电一段时间后,KOH的物质的量浓度不发生变化
D.通甲烷极的电极反应式是:CH4+10OH-=CO32-+7H2O+8e-
5.碱性锌锰干电池在放电时,电池总反应方程式可以表示为:Zn+2MnO2+H2O=Zn(OH)2
+2MnOOH,在此电池放电时,正极(碳棒)上发生反应的物质是 ( )
A. Zn B. 碳棒 C. MnO2 D.MnOOH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com