
题目列表(包括答案和解析)
6.mg铜和足量硝酸溶液反应,生成VL气体(标准状况),则反应中发生转移的电子的物质的量最接近于 ( )
A.m/16 mol B.m/22.4 mol
C.m/32 mol D.m/11.2 mol
5.在一定温度和压强下,将一容积15ml的试管充满NO2后,倒置于一个盛水的水槽中。当试管内液面上升至一定高度不再变化时,在相同条件下再通入O2,若要使试管内液面仍保持在原高度,则应通入O2体积为 ( )
A.3.75ml B.7.5ml C.8.75ml D.10.5ml
4.五氧化二磷不仅是一种强干燥剂干而且有很强的脱水性,向浓硝酸中加入过量的P2O5,
能生成一种含氮化合物M,则M最可能是 ( )
A.N2 B.NO2 C.NO D.N2O5
3.下列所叙述的现象与人类活动造成的环境污染无关的是 ( )
A.地球表面产生的光化学烟雾
B.地球大气外层出现的臭氧层空洞
C.下雨时电闪雷鸣产生的氮氧化物
D.下雨时出现的酸雨
2.把Al粉和下列氮的气态氧化物混合后,加热至高温,均可生成氮气和氧化铝。若反应后气体体积是反应前气体体积的一半(同温同压条件下测得),则氮的氧化物是 ( )
A.NO B.N2O3 C.N2O4 D.N2O5
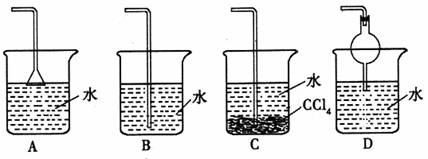
1.已知NH3难溶于CCl4,如图所示,下列装置中,不适宜于NH3气体尾气吸收的是( )
21.(9分)将N2和H2按一定比例混合,在相同状况下其密度为H2密度的3.6倍。取1mol该混合气体盛入密闭容器内,使之发生反应并在一定条件下达到平衡。已知反应达到平衡后容器内的压强是相同条件下反应前压强的0.76倍。试求:
(1)反应前混合气体中N2和H2的体积比
(2)达到平衡时混合气体中氨的物质的量
20.(10分)在一个固定体积的密闭容器中,向容器内充入2molA和1molB,发生如下反应:2A(g)+B(g) 3C(g)+D(s),反应达到平衡时C的物质的量浓度为1.2mol/L。
3C(g)+D(s),反应达到平衡时C的物质的量浓度为1.2mol/L。
(1)该反应的平衡常数表达式K= ,若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为 (填“吸热”或“放热”)反应,反应的平衡常数K (填“增大”“减小”或“不变”)。
(2)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2mol/L的是 (用序号填空)
① 4molA + 2molB ② 3molC + 1molD + 1molB
③ 3molC + 2molD ④ 1.6molA + 0.8molB + 0.6molC
(3)若向容器内加入3molC和0.8molD,反应达到平衡时C的浓度仍为1.2mol/L,则容器的容积V应大于 L,小于 L。
19.(10分)在一固定体积的密闭容器中,在900℃时发生反应:
CH4(g)+H2O(g) CH3OH(g)+H2(g);△H=-Q KJ/mol(Q>0)。容器内各物质的浓度(mol/L)变化如下:(在900℃其化学平衡常数K=1.0)
CH3OH(g)+H2(g);△H=-Q KJ/mol(Q>0)。容器内各物质的浓度(mol/L)变化如下:(在900℃其化学平衡常数K=1.0)
|
时间/min |
CH4 |
H2O |
CH3OH |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是 。
A.容器内压强不变 B.v正(H2)=v逆(CH4)
C.混合气体中CH3OH的浓度不变 D.c(CH3OH)=c(CH4)
(2)若在900℃时向反应容器中充入H2O,K值 (填“增大”“减小”或“不变”,下同);若升高反应体系的温度,K值 。
(3)上表中:c1= mol/L,H2O的转化率为 。
18.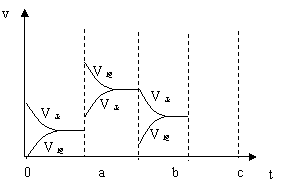 (12分)Ⅰ.下图是表示在密闭容器中反应:2SO2+O2
(12分)Ⅰ.下图是表示在密闭容器中反应:2SO2+O2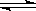 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是 ;b
c过程中改变的条件可能是 ;
若增大压强时,反应速度变化情况画在c~d处。
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a b过程中改变的条件可能是 ;b
c过程中改变的条件可能是 ;
若增大压强时,反应速度变化情况画在c~d处。
Ⅱ.在一个固定体积的密闭容器中,加入2 mol A和1 mol B,发生反应:
2A(g)+B(g) 3C(g)+D(g)达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度
3C(g)+D(g)达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度
(填“大于”“小于”或“等于”)。
(1)加入2mol A、1mol B、3mol C、1mol D时,C的平衡浓度________Wmol·L-1。
(2)加入3 mol C和1 mol D时,C的平衡浓度_________Wmol·L-1。
(3)加入2 mol B、3 mol C、1 mol D时,C的平衡浓度_________Wmol·L-1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com