
题目列表(包括答案和解析)
15.σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成。则下列分子中的σ键是由两个原子的s、p轨道以“头碰头”方式重叠构建而成的是 ( )
A.H2 B.Cl2 C. NaH D.HF
14.下列性质中,能充分说明某晶体是离子晶体的是 ( )
A.具有较高的熔点 B.固态不导电,水溶液能导电
C.可溶于水 D.固态不导电,熔融状态能导电
13.下列叙述正确的是 ( )
A.氯化钠晶体不能导电,所以氯化钠不是电解质
B.氯化钠溶液能导电,所以氯化钠溶液是电解质
C.熔融的氯化钠和氯化钠溶液都能产生自由移动的离子
D.氯化钠熔融时不破坏氯化钠晶体中的离子键。
12.金属的下列性质中,与自由电子无关的是()
A.易导热 B.容易导电 C.延展性好 D.密度大小
11.既有离子键又有配位键的化合物是 ( )
A.NH4NO3 B.NaOH C.H2SO4 D.H2O
10.下列分子含有的电子数目与HF相同,且只有两个极性共价键的是
A.CO2 B.N2O C.H2O D.CH4
9.某原子核外共有6个电子,分布在K与L电子层上,在下列L层分布中正确的是 A.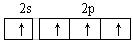 B.
B.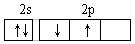
C.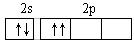 D.
D.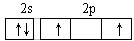
8.金属键的强弱与金属价电子数的多少有关,价电子数越多金属键越强,与金属阳离子的半径大小也有关,金属阳离子的半径越大,金属键越弱。据此判断下列金属熔点逐渐升高的( )
A.Li Na K B.Na Mg Al C.Li Be Mg D.Li Na Mg
7. 下列按电负性减小顺序排列的是 ( )
A . K、Na、Li B. As、P、N C. N、O、F D. O、S、Se
6.下列说法中正确的是:
A.随原子序数的递增,第三周期元素的电负性逐渐减小
B.铝的第一电离能比镁的第一电离能大
C.在所有的元素中,氟的第一电离能最大
D.在所有的元素中,氟的电负性最大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com