
题目列表(包括答案和解析)
19.灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s、灰) Sn(s、白)
△H3=+2.1kJ/mol
Sn(s、白)
△H3=+2.1kJ/mol
下列说法正确的是
A.△H1>△H2 B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
18.下列反应属于放热反应的是
A.氢气还原氧化铜 B.葡萄糖在人体内氧化分解
C.Ba(OH)2·8H2O与NH4Cl反应 D.氢氧化钾和硫酸中和
17.已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-Q1KJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H=-Q2KJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H=-Q3KJ·mol-1
常温下,取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到到常温,放出的热量(单位:KJ)为
A、0.4Q1+0.05Q3 B、0.4Q1+0.05Q2 C、0.4Q1+0.1Q3 D、0.4Q1+0.2Q3
16.1g氢气完全燃烧生成液态水放出142.9kJ的热量, 则下列热化学方程式中, 正确的是
A.H2O(l )=H2(g) +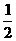 O2(g) △H =+285.8kJ/mol
O2(g) △H =+285.8kJ/mol
B.2 H2(g) + O2(g) = 2 H2O(l) △H =-571.6kJ/mol
C.2 H2 + O2 = 2 H2O △H =-571.6kJ/mol
D.2 H2(g) + O2(g) = 2 H2O(l) △H =-142.9kJ/mol
15.已知下列热化学方程式:
①Fe3O4(S)+ CO(g)= 3FeO(s)+ CO2(g) ΔH1= ― 36.5Kj/mol
②Fe2O3(S)+ 3CO(g)= 2Fe(s)+ 3CO2(g) ΔH2= ― 26.7Kj/mol
③3Fe2O3(S)+ CO(g)= 2 Fe3O4+ CO2(g) ΔH3= ― 50.75Kj/mol
则反应FeO(s)+ CO(g)= Fe(s)+ CO2(g)的焓变
A. +7.28kJ/mol B. ―7.28kJ/mol C. +43.65 kJ /mol D.―43.65K kJ /mol
14.在36 g 碳不完全燃烧所得气体中,CO占1/3体积,CO2占2/3体积,且
C(s) + 1/2O2(g) = CO(g) △H = -110.5 kJ/mol
CO(g) + 1/2O2(g) = CO2(g) △H = -283 kJ/mol
与这些碳完全燃烧相比,损失的热量是
A.172.5 kJ B. 1149 kJ C.283kJ D. 517.5 kJ
13.下列各组热化学方程式中,化学反应的△H前者大于后者的是
A.C(s)+O2(g) =CO2(g) △H1 C(s)+O2(g) =CO(g) △H2
B.S(s)+O2(g) =SO2(g) △H3 S(g)+O2(g) =SO2(g) △H4
C. 2H2(g)+O2(g=2H2O(l) △H5 H2(g)+O2(g) =H2O(l) △H6
D.CaCO3(s) =CaO(s)+CO2(g) △H7 CaO(s)+H2O(l) =Ca(OH)2(s) △H8
12.下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反映的中和热△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的△H=2×283.0kJ/mol
C.需要加热才能发生的反应不一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
11.已知:(1)Zn(s)+1/2O2(g)==ZnO(s) ΔH1 = -348.3kJ/mol
(2)2Ag(s)+1/2 O2(g)== Ag2O(s) ΔH2 = -31.0kJ/mol
则Zn(s)+ Ag2O(s) == ZnO(s) + 2Ag(s) ΔH3 中 ,ΔH3等于
A.-332.8 kJ/mol B.-379.3kJ/mol C.-317.3kJ/mol D.317.3 kJ/mol
10.已知在25℃、1×105 Pa时,石墨、CO的燃烧热分别是393.5 kJ·mol-1和283.0 KJ·mol-1,下列说法或方程式正确的是
A、在相同条件下:2C(石墨)+O2(g)=2CO(g);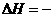 110.5 kJ·mol-1
110.5 kJ·mol-1
B、1 mol石墨不完全燃烧,生成CO2和CO混合气体时,放热504.0 kJ
C、在相同条件下:C(石墨)+CO2(g)=2CO(g);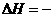 172.5 kJ·mol-1
172.5 kJ·mol-1
D、若金刚石的燃烧热大于石墨的燃烧热,则石墨转变为金刚石需要吸热
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com