
题目列表(包括答案和解析)
7、镀锌铁在发生析氢腐蚀时,若有0.2mol电子发生转移,下列说法正确的是:
①有5.6g金属被腐蚀 ②有6.5g金属被腐蚀 ③在标准状况下有2.24L气体放
出 ④在标准状况下有1.12L气体放出
A、①② B、②③ C、①④ D、③④
6.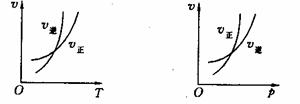
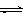 可逆反应mA(g) nB(g)+pC(s) △H=Q, 温度和压强的变化对正、逆反应速率的影响分别符合右图中的两个图像,以下叙述正确的是:
可逆反应mA(g) nB(g)+pC(s) △H=Q, 温度和压强的变化对正、逆反应速率的影响分别符合右图中的两个图像,以下叙述正确的是:
A、m>n, Q>0
B、m>n+p,Q>0
C、m>n,Q<0
D、m<n+p, Q <0
5、下列叙述中,正确的是
①锌跟稀硫酸反应制取氢气,加入少量CuSO4溶液能提高反应速率 ②镀层破损后,白铁(镀锌的铁)比马口铁(铁锡的铁)更易腐蚀 ③电镀时应把镀件置于电解槽的阴极 ④冶炼铝时,把氧化铝加热成为熔融体后电解 ⑤钢铁表面常易腐蚀生成Fe2O3·nH2O
A.①②③④⑤ B.①③④⑤ C.①③⑤ D.②④
4、在一个绝热的体积一定的密闭容器中发生可逆反应:
N2(g) + 3H2(g)
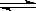 2NH3(g)△H<0 下列各项中不能说明该反应已经达到平衡状态的是
A.体系的压强不再改变
B.体系的温度不再改变
C.断裂1mol N≡N键的同时,也断裂6molN-H键
D.反应消耗的 、与产生的的速率υ() : υ() : υ() == 1∶3 ∶2
2NH3(g)△H<0 下列各项中不能说明该反应已经达到平衡状态的是
A.体系的压强不再改变
B.体系的温度不再改变
C.断裂1mol N≡N键的同时,也断裂6molN-H键
D.反应消耗的 、与产生的的速率υ() : υ() : υ() == 1∶3 ∶2
3.已知下列热化学方程式:
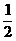 CH4(g)+O2(g)===
CH4(g)+O2(g)===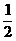 CO2(g)+H2O(1)
△H= -445.15kJ·mol-1
CO2(g)+H2O(1)
△H= -445.15kJ·mol-1
CH4(g)+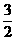 O2(g)====CO(g) + 2H2O(1) △H= -607.3KJ·mol-1
O2(g)====CO(g) + 2H2O(1) △H= -607.3KJ·mol-1
CH4(g)+ 2O2(g) ====CO2(g)+2H2O(1) △H= -890.3KJ·mol-1
CH4(g)+ 2O2(g) ====CO2(g)+2H2O(g) △H= -802.3KJ·mol-1
则CH4的燃烧热为:
A、445.15kJ·mol-1 B、607.3KJ·mol-1 C、890.3KJ·mol-1 D、802.3KJ·mol-1
2.下列关于化学反应的自发性叙述中正确的是
A.焓变小于0而熵变大于0的反应肯定是自发的
B.焓变和熵变都小于0的反应肯定是自发的
C.焓变和熵变都大于0的反应肯定是自发的
D.熵变小于0而焓变大于0的反应肯定是自发的
1.2007年3月温家宝总理在十届全国人大五次会议上提出“要大力抓好节能降耗、保护环境”,下列举措中违背了这一指导思想的是
A.加大开发太阳能、水能、风能、地热能等能源力度,减少化石燃料的使用
B.研制乙醇汽油(汽油中添加一定比例的乙醇)技术,降低机动车辆尾气中有害气体排放
C.生产、生活中,努力实现资源的循环利用
D.利用高新技术,提高石油、煤、天然气产量,以满足工业生产快速发展的需求
26.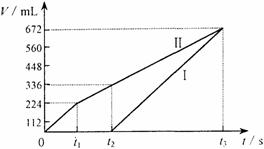 (9分)常温下电解200 mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如右图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(1)原混合溶液NaCl和CuSO4的物质的量浓度。
(2)t2时所得溶液的c(H+)。
(3)电解至t3时,消耗水的质量。
(9分)常温下电解200 mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如右图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:(1)原混合溶液NaCl和CuSO4的物质的量浓度。
(2)t2时所得溶液的c(H+)。
(3)电解至t3时,消耗水的质量。
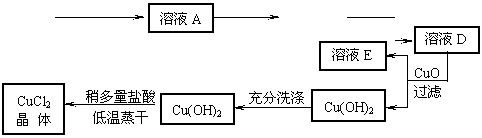
25.(8分)工业上制取CuCl2的生产流程如下:
|
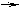

|
|
|
|
|
请结合下表数据,回答下列问题:
|
物 质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
|
溶度积/25℃ |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
|
完全沉淀时的pH范围 |
≥9.6 |
≥6.4 |
3-4 |
⑴ 向含有等浓度Fe2+、Cu2+、Fe3+的混合溶液中滴加NaOH溶液,最先生成的沉淀是 。
⑵ 溶液A中加入NaClO的目的是 。
⑶ 在溶液B中加入CuO后过滤,这次过滤控制的条件是 。
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
24.(12分)在温度t℃下,某Ba(OH)2的稀溶液中c(H+)=10-5mol·L-1,c(OH-)=10-1mol·L-1,已知a+b=12,向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示
|
序号 |
氢氧化钡的体积/mL |
盐酸的体积/mL |
溶液pH |
|
(1) |
22.00 |
0.00 |
8 |
|
(2) |
22.00 |
18.00 |
7 |
|
(3) |
22.00 |
22.00 |
6 |
(1)依据题意判断,t℃_______25℃(填大于、小于、等于),该温度下水的离子积Kw=______。
(2)b=__________,原Ba(OH)2的稀溶液的物质的量浓度为__________。
(3)向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀达最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为________以及其中Na2SO4的物质的量浓度为__________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com