
题目列表(包括答案和解析)
24.(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3- +4H++3e- = NO+2H2O; KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:________________________________。
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是 mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: 。
(以上试题答案务必答在答题卷上面每题对应的答题区域内,否则不得分)
 2008-2009学年长葛三高第一次考试试卷
2008-2009学年长葛三高第一次考试试卷
|
座号 |
|
高二化学 命题人:李新朵
说明:1.答题前请将密封线内各项内容填写清楚。
23.(8分)已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
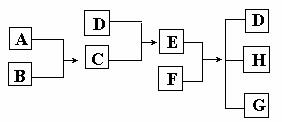
⑴ D的化学式(分子式)是____________,E的化学式(分子式)是_____________。
⑵ A和B反应生成C的化学方程式是___________________________________。
⑶ E和F反应生成D、H和G的化学方程式是_____________________________。
22.(10分)请回答有关氨气的问题。
(1)实验室常用下列的装置和选用的试剂制取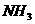 ,其中正确的是 (填序号)。
,其中正确的是 (填序号)。
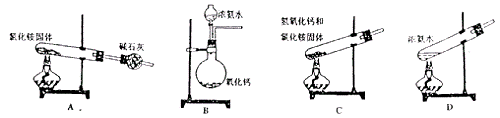
(2)若实验室收集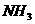 要采用___________________________法。
要采用___________________________法。
(3)若检验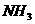 ,可用___________________________。
,可用___________________________。
(4)氨气电子式为_____________________,结构式为_____________________。
21.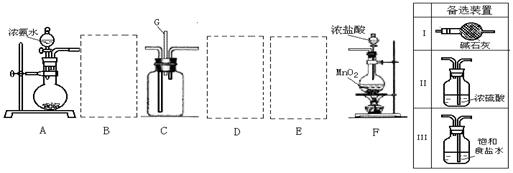 (12分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
(12分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置F中发生反应的离子方程式 。
(2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择。并将编号填入下列空格。 B__________ D__________ E__________(均填编号)
(4)氯气和氨气在常温下相混就会反应生成氯化铵和氮气,装置C内出现浓厚的白烟并在容器内壁凝结,请设计实验方案鉴定该固体就是氯化铵:
。
(5)从装置C的出气管口处逸出的尾气可能含有污染环境的气体,如何处理?
。
20.一定质量的铜和足量的硝酸反应,所放出的气体与标准状况下的氧气1.12L混合后再通入水中,恰好被完全吸收,则铜的质量为( )
A.3.2g B.4.8g C.6.4g D.10.8g
第Ⅱ卷(非选择题 共40分)
19.取三张蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加65%的HNO3、98.3%的H2SO4和新制的氯水,三张试纸最后依次呈现的颜色是( )
A.白、红、白 B.红、黑、红 C.红、红、红 D.白、黑、白
18.(NH4)2SO4在高温下分解,产物是 SO2、H2O、N2和 NH3。在该反应的化学方程式中,化学计量数由小到大的产物分子依次是( )
A.SO2、H2O、N2、NH3 B.N2、SO2、H2O、NH3
C.N2、SO2、NH3 、H2O D.H2O、NH3、SO2、N2
17.木炭屑与浓HNO3共热,产生的气体等分为①和②两份,将第一份气体先导入适量蒸馏水中再导入石灰水中,将第二份气体直接导入石灰水中,则石灰水的变化可能是( )
A.①不变浑浊②变乳白色 B.①变乳白色②不变浑浊
C.①变乳白色②变乳白色 D.①不变浑浊②变浅黄色
16.在检验金首饰是否用纯金(可能含有铜或银)制成,可把样品浸于某溶液一段时间后取出,根据质量是否变化即可判断。可以选用的溶液是( )
A. 盐酸 B. 硫酸 C. 硝酸 D. 氢氧化钠溶液
15.锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为( )
A.2mol B.1 mol C.0.5mol D.0.25mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com