
题目列表(包括答案和解析)
14. 醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
A、醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B、0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小
C、CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D、常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH=7
第Ⅱ卷(共72分)
13.在相同温度和压强下,对反应CO2(g)+H2(g)=CO(g)+H2O (g)进行甲、乙、丙、丁四组实验,,实验起始时放入容器内各组分的物质的量见下表
|
物质的量 |
CO2 |
H2 |
CO |
H2O |
|
甲 |
a mol |
a mol |
0 mol |
0 mol |
|
乙 |
2a mol |
a mol |
0 mol |
0 mol |
|
丙 |
0 mol |
0 mol |
a mol |
a mol |
|
丁 |
a mol |
0 mol |
a mol |
a mol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A.乙=丁>丙=甲 B乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
12.根据下列有关图象,说法正确的是

A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0
B.由图Ⅱ知,反应在t6时,NH3体积分数最大
C.由图Ⅱ知,t3时采取降低反应温度的措施
D.Ⅲ在10L容器、850℃时反应,由图知,到4min时,反应放出51.6kJ的热量
11.在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g) xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是
A.若平衡时,甲、乙两容器中A的物质的量不相等,则x=4
B.平衡时,甲、乙两容器中A、B的物质的量之比不相等
C.平衡时甲中A的体积分数为40%
D.若平衡时两容器中的压强不相等,则两容器中压强之比为8∶5
10.下列表格中的各种情况,可以用下面对应选项中的图像曲线表示的是( )
|
选项 |
反应 |
纵坐标 |
甲 |
乙 |
|
A |
外形、大小相近的金属和水反应 |
反应速率 |
K |
Na |
|
B |
4mL0.01mol/L的KMnO4溶液,分别和不同浓度的H2C2O4(草酸)溶液各2mL反应 |
0.1mol/L的 H2C2O4溶液 |
0.2mol/L 的H2C2O4溶液 |
|
|
C |
5mL0.1mol/LNa2S2O3溶液和5mL0.1mol/LH2SO4溶液反应 |
热水 |
冷水 |
|
|
D |
5mL4%的过氧化氢溶液分解放出O2 |
无MnO2粉末 |
加MnO2粉末 |

9.反应A2+B2 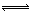 2AB在不同温度和压强改变条件下,产物AB的生成情况,如图所示:a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是( )
2AB在不同温度和压强改变条件下,产物AB的生成情况,如图所示:a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是( )
A.A2、B2、AB均为气体,正反应放热
B.AB为气体,A2、B2中最少有一种为非气体,正反应放热
C.AB为气体,A2、B2中最少有一种为非气体,正反应吸热
D.AB为固体,A2、B2中最少有一种为非气体,正反应吸热
8.取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的PH等于12,则原溶液的浓度为
A.0.01mol/L B. 0.017mol/L C. 0.05mol/L D. 0.50mol/L
7.下列变化为放热的化学反应的是
A.H2O(g)=H2O(l) △H=-44.0 kJ/mol
B.2HI(g)=H2(g)+I2(g) △H=+14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
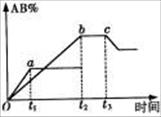
D.能量变化如右图所示的化学反应
6.甲醇广泛用作燃料电池的燃料,可出天然气来合成,已知:
①2CH4(g)+O2(g)=2CO(g)+4H2(g) △H=-71kJ/mol
②CO(g)+2H2(g)=CH3OH(l) △H=-90.5kJ/mol
③CH4(g)+2O2(g)=CO2+2H2O(g) △H=-890kJ/mol
下列说法不能得出的结论是
A、反应②在任何温度下均能自发进行
B.CO(g)+2H2(g)=CH3OH(g)△H>-90.5kJ/mol
C.甲醇的燃烧热为764kJ/mol
D、若CO的燃烧热为282.5kJ/mol,则H2的燃烧热为286kJ/mol
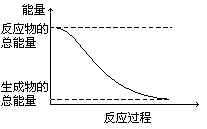
5.将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)  2HBr(g)
2HBr(g)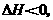 g平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
g平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是( )
A.a>b B.a=b C.a<b D.无法确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com