
题目列表(包括答案和解析)
20. (6分)
 mA(气) + nB(气)
mA(气) + nB(气) 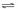 pC(气) + qD(气)
pC(气) + qD(气)
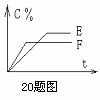
的 C % 与时间 t 有如图关系
⑴ 若E、F表示两种温度,则 E____F ( 填 > 、< 或 = ),正反应_ __ 热
 ⑵ 若E、F表示两种压强,则 m + n_____p + q
⑵ 若E、F表示两种压强,则 m + n_____p + q
19、(8分)
(1)、化学反应过程中都伴随着能量变化,反应热是指化学反应过程中所______
或_______的热量。符号:______,单位:______________;反应热的来源,主要是旧化学键的_______和新化学键的_________所发生的能量变化.一个反应是放热还是吸热决定于______________和______________的高低。
(2)、在25℃、101KPa时,____________________________的化合物时所放出的热量,叫做该反应的燃烧热;在250C、101KPa时,1克甲醇(CH30H)完全燃烧
生成CO2和液态水时放热22.68KJ,则能表示甲醇燃烧热的热化学方程式为
_________________________________________________________________
18、 (4分)
(4分)
 (1)、据了解,我国兴建的三峡工程提供的水力发电功率相当于3000万kW的火力发电站。因此,三峡建设将有助于控制
(1)、据了解,我国兴建的三峡工程提供的水力发电功率相当于3000万kW的火力发电站。因此,三峡建设将有助于控制
A. 温室效应 B. 白色污染
C. 城市污水的任意排放 D. 长江中、下游的洪涝灾害
(2)、已知1 g碳粉在氧气中完全燃烧放出的热量是32.8 kJ(与1g 原煤相当)试写出相关的热化学式: 。
17.某温度下在密闭容器中发生如下反应: 2M(g)+ N(g) 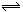 2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为
2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为
A.20% B.40% C.60% D. 80%
郯城一中高二期中考试
化 学(理科班) 2008-11-3
第Ⅱ卷 (共49分)
16.以下反应可以用熵判据来解释的是( )
A.硫酸铜饱和溶液降低温度时有晶体析出
B.CaO(s)+CO2(g)==CaCO3(s) △H=-175.7kJ/mol
C.(NH4)2CO3(s)==NH4HCO3(s)+NH3(g) △H=+74.9kJ/mol
D.2H2(g)+O2(g)==2H2O(l) △H=-285.8kJ/mol
15.在两个恒容容器中有平衡体系:A(g) 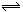 2B(g)和2C(g)
2B(g)和2C(g)
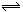 D(g),X1和X2分别是A和C的转化率。在温度不变情况下,均增加相同的A和C的物质的量,下列判断正确的是:
D(g),X1和X2分别是A和C的转化率。在温度不变情况下,均增加相同的A和C的物质的量,下列判断正确的是:
A.X1降低,X2增大 B.X1、X2均降低
C.X1增大,X2降低 D.X1、X2均增大
14.一定温度下,可逆反应A2(s)+3B2(g) 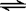 2AB3(g)达到平衡的标志是
2AB3(g)达到平衡的标志是
A.容器内每减少1mol A2,同时生成2mol AB3
B.容器内每减少1mol A2,同时消耗3mol B2
C.参加反应的总的物质的量始终在变化。
D.容器内的气体密度不再改变
13.在密闭容器中,有可逆反应:nA(气)+mB(气)  pC(气)处于平衡状态(已知m+n>p,△H>0)下列说法中正确的是
pC(气)处于平衡状态(已知m+n>p,△H>0)下列说法中正确的是
①升高温度时,[B]/[C]的值减小;②降温时,体系内混合气体的平均摩尔质量减小;③加入B后,A的转化率变大;④加入催化剂,气体总物质的量不变;⑤充入C后,A,B的物质的量增大.
A.③④ B.②③⑤ C.①②⑤ D.全部
12.下列热化学方程式中,△H能正确表示物质的燃烧热的是
A.CO(g) +1/2O2(g) ==CO2(g); △H=-283.0 kJ/mol
B C(s) +1/2O2(g) ==CO(g); △H=-110.5 kJ/mol
C. H2(g) +1/2O2(g)==H2O(g); △H=-241.8 kJ/mol
D.2C8H18(l) +25O2(g)==16CO2(g)+18H2O(l); △H=-11036 kJ/mol
11.已知:C(s,金刚石)=C(s,石墨)△H=-1.9KJ/mol
C(s,金刚石)+O2(g)=CO2(g) △H1
C(s,石墨)+O2(g)=CO2(g) △H2
根据已述反应所得出的结论正确的是
A、△H1=△H2 B、△H1>△H2
C、△H1<△H2 D、金刚石比石墨稳定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com