
题目列表(包括答案和解析)
2、2008年6月1日,国家有关部门下达了“限塑令”,从即日起全国各商场对包装用塑料袋实行收费。这一政策出台的目的是
A、提高经济收入 B、控制和减少白色污染 C、节约能源 D、资助地震灾区
1、2008年9月国家有关部门检出了以三鹿婴幼儿奶粉为首的一批奶制品中掺和的三聚氰胺,并立即对全国的这些奶制品加以封存或销毁。三聚氰胺本是一种优良的化工原料,主要用来制涂料和黏合剂,它的相对分子质量介于100与200之间,碳的质量分数为28.57%,碳、氢的质量比为6:1,其余为氮。则三聚氰胺的分子式为
A、(CH2N2)n B、C3H4ON5 C、C3H6N6 D、C4H4N5
21.(8分)在一定条件下,可逆反应:mA+nB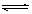 pC达到平衡,若:
pC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则m+n和p的关系是 。
(2)A、C是气体,增加B的量,平衡不移动,则B为 态。
(3)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是 。
(4)加热后,可使C的质量增加,则正反应是 反应(放热或吸热)。
20.(9分)
10 0C时加热NaHCO3饱和溶液,测得该溶液的PH发生如下变化:
|
温度(0C) |
10 |
20 |
30 |
加热煮沸后冷却到50 0C |
|
PH |
8.3 |
8.4 |
8.5 |
8.8 |
甲认为,该溶液的PH升高的原因是HCO3-离子的水解程度增大,所以碱性增强,该反应的离子方程式为 ;乙认为,溶液PH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”) NaHCO3。丙认为甲、乙的判断都不准确,丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,如果产生白色沉淀,则 (填“甲”或“乙”)判断正确,该试剂是 (填编号)
A.氢氧化钡溶液 B.氯化钡溶液 C.氢氧化钠溶液 D.澄清石灰水
(2)将加热后的溶液冷却到10 0C,若溶液的PH等于8.3,则 (填“甲”或“乙”)。
(3)查阅资料发现,NaHCO3的分解温度为1500C,丙断言 (填“甲”或“乙”)的判断是错误的,理由是 。
19.(15分)
(1)相同物质的量浓度下的各溶液:NaX、NaY、NaZ,其PH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序为: ______
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是 _____
(3)写出Na2CO3在水中的电离方程式: _________________________________________
(4)写出氯化铁溶液水解反应的离子方程式,并判断溶液的酸碱性:
______________________________________溶液显_______性
18.(10分)
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)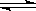 CO(g)+H2O(g)
CO(g)+H2O(g)
其化学平衡常数K和温度t的关系如下表:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
(a)容器中压强不变 (b)混合气体中 c(CO)不变
(c)v正(H2)=v逆(H2O) (d)c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
17.(10分)
将气体A、B置于容积为2L的密闭容器,发生如下反应:
4A(g)+B(g)=2C(g)
反应进行到4S末,测得A为0.5mol,B为0.4mol,C为0.2mol,
(1)则vA= _____________ vB= _________________ vC= ______________
(2)反应前A有 ___ mol,反应前B有 _____ mol
16.在氯化铵溶液中,下列关系式正确的是 ( )
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.c(NH4+)> c(Cl-)>c(H+)>c(OH-)
C.c(Cl-)=c(NH4+)>c(H+)=c(OH-)
D.c(NH4+)= c(Cl-)>c(H+)>c(OH-)
15. 95℃时,水中的H+的物质的量浓度为1×10-6mol·L-1,若把0.01mol的NaOH固体溶解于
95℃水中配成1L溶液,则溶液的pH为
A.2 B.4 C.10 D.12
14.在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是 ( )
A.CH3OH(l)+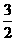 O2(g)
O2(g) CO2(g)+2H2O(l) △H=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(l) △H=-1452
kJ/mol
C.2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(l) △H=-725.8
kJ/mol
D.2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(l) △H=+1452 kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com