
题目列表(包括答案和解析)
19. ⑴ 。 ⑵ ⑶
⑷① 。
② 。
18. (1) 。
(2) 。
(3) 。
17. (1)A1___ ____A2___ ____B1____ ___B2__________.
(2) ______ _________.
(3)
___________________________________________________________________.
(4) ______ ___________.
16. ⑴
⑵ ① 。
② 。 。
⑶ 。
15(1)① 。 , ,
。
② 。
③ , 。 。
(2)
(3)
0.05mol的气体时,CuSO4恰好被完全电解,得密度为1.2g/cm3的溶液200mL,求:
(1)电解后所得溶液的pH.
(2)电解前所取CuSO4溶液的质量.
(3)若要使电解后所得溶液恢复至电解前的原状态,需要加入一种什么物质,质量为多少克?


 高二化学月考答卷(选修)
高二化学月考答卷(选修)
21. (12分)某温度下,取一定质量的硫酸铜溶液,用石墨作电极进行电解,当阳极产生
20.(8分)有甲乙两个容积均为1L的密闭容器,在控制两容器的温度相同且恒定的情况下进行反应:2A(g)+B(g) 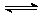 xC(g),①向甲中通入4molA、2molB,达平衡时测得其中C的体积分数为40%;②向乙中通入1molA、0.5molB和3molC,平衡时测得C的体积分数为W%。试回答:
xC(g),①向甲中通入4molA、2molB,达平衡时测得其中C的体积分数为40%;②向乙中通入1molA、0.5molB和3molC,平衡时测得C的体积分数为W%。试回答:
(1)甲平衡时A的体积分数为 ;
(2)若乙W%=40%,且建立平衡的过程中乙压强有变化 ,则x= ,乙中建立平衡时压强的变化为 (填“递增”或“递减”)。
(3)若乙W%=40%,且平衡时甲、乙压强不同,则x= ,平衡时甲的压强 乙的压强(填“大于”或“小于”),乙平衡时c(A)平= 。
(4)若x=4,则W% 40% (填“大于”、“小于”或“等于”,下同);平衡时乙中的c(A)
甲中的c(A)。
19.(10分)一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)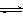 FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
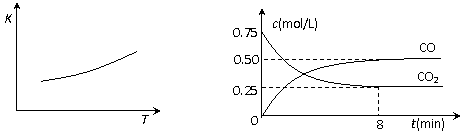
图甲 图乙
⑴该反应的平衡常数表达式K= 。
⑵一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图乙所示。
8分钟内,CO的平均反应速率v(CO)= mol/(L·min)。
⑶下列措施中能使平衡时c(CO)/c(CO2)增大的是 (填序号)。
A.升高温度 B.增大压强
C.充入一定量CO D.再加入一些铁粉
⑷铁的重要化合物高铁酸钠是一种新型饮用水消毒剂,具有氧化能力强、安全性好等优点。
①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O
 Na2FeO4+3H2↑,则电解时阳极的电极反应式是 。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是 。
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化纳和水,该反应的离子方程式为 。
18.(6分)已知:在热力学标准态(298K、1.01×105Pa)下,
由稳定的单质发生反应生成1mol化合物的反应热叫该化合物
的生成热(△H)。右图为氧族元素氢化物a、b、c、d的生成
热数据示意图。试回答下列问题:
(1)写出氧族元素中含有18e-的两种氢化物的电子式
。
(2)请你归纳:非金属元素氢化物的稳定性与氢化物的反应
热△H的关系
。
(3)写出硒化氢在热力学标准态下,发生分解反应的热化学反应方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com