
题目列表(包括答案和解析)
2. 瑞士化学家盖斯,根据一系列事实于1840年提出:不管化学反应是一步或分数步完成,这一过程的热效应相同。换言之,若一个反应可分成几步反应完成,则各步反应的反应热总和与该反应一次发生时反应热相同。应用这个原理,已知:C(s)+O2(g)=CO2(g) ∆H= -393.5kJ/mol;CO(g)+1/2 O2(g)=CO2(g) ∆H= -283kJ/mol;则C(s)与O2(g)反应生成1molCO(g)的反应热为 ( )
A. ∆H= -676.5kJ/mol B. ∆H= +676.5kJ/mol
C. ∆H= -110.5kJ/mol D.∆H= +110.5kJ/mol
1.在北京奥运会期间,氢燃料电池公交汽车已经驶上北京街头,体现“科技奥运,绿色奥运”。下列说法正确的( )
A.电解水制取氢气是理想而经济的制氢方法
B.发展氢燃料电池汽车不需要安全高效的储氢技术
C.氢燃料电池把氢气和氧气燃烧放出的热能转化为电能
D.氢燃料电池汽车的使用可以有效减少城市空气污染
30.(本题共10分)如右图所示,将6 mol X和3 mol Y混合气体置于体积可变的等压容器中,在一定温度下发生如下反应:
2X(g)+Y(g) 2Z(g)。
2Z(g)。
 反应达到平衡状态A时,测得气体总物质的量为6.6
mol。
反应达到平衡状态A时,测得气体总物质的量为6.6
mol。
若X、Y、Z的起始物质的量分别用A.B.c表示,回答下列问题:
(1)达平衡状态A时,Y的转化率为____________,在达到平衡状
态A的容器中通人少量Y,体系中X的体积分数_____________(填“增大”或“减小”或“不变”)。
(2)若起始时a=3.2 mol,且达到平衡后各气体的体积分数与平衡状态A相同,则起始时B.c的取值分别为b___________________;c_______________________。
(3)若要使反应开始时向逆反应方向进行,且达到平衡后各气体的物质的量与平衡状态A相同,则起始时c的取值范围是__________________________。
29.(本题共6分)在一密闭容器中投入一定量的A和B发生如下反应:mA(g)+nB(g) pC(g)+qD(g)。
pC(g)+qD(g)。
(1)若反应达到化学平衡时,A与B的转化率相等,则起始时投入的A与B的物质的量之比为_____________________。
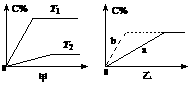 (2)相同的压强下,充入A.B后,分别在温度
(2)相同的压强下,充入A.B后,分别在温度
T1和T2条件下生成的C在反应混合物中的
百分含量与时间的关系如图甲所示。
则T1________T2(填“>”、“<”或“=”),
该反应的正反应为_________(填“吸热”或
“放热”)反应。
(3)如图乙所示,曲线a代表一定条件下该反应的进程。若使曲线a变为曲线b,可能采取的措施是___________________________或___________________________。
28.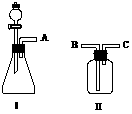 (本题共10分)如图所示,Ⅰ为中学化学常用的气体
(本题共10分)如图所示,Ⅰ为中学化学常用的气体
发生装置,Ⅱ(不能上下颠倒)为气体收集装置。现
提供如下试剂:①NH4Cl和Ca(OH)2的固体混合物;
②双氧水、MnO2固体;③KClO3和MnO2固体;
④浓氨水、生石灰固体。
(1)现用装置Ⅰ制备O2,选用的试剂是_____________(填序号)。发生反应的化学方程式是__________________________。收集O2时,导管的连接方法是A接________。根据你所学的知识,写出用装置Ⅰ制O2的另一个反应的化学方程式__________________________。
(2)现用装置Ⅰ制备NH3,选用的试剂是_____________(填序号)。发生反应的化学方程式是_____________________________。收集NH3时,导管的连接方法是A接_________。
27.(本题共6分)某无色混合气体可能含有CO2、CO、NH3、N2、HCl、H2中的一种或几种,依次进行以下处理(假设每次处理均反应完全):①通过浓硫酸时,气体体积缩小;②通过碱石灰时,气体体积缩小;③通过炽热的氧化铜时,固体变为红色;④通过白色硫酸铜粉末时,粉末变为蓝色;⑤通过澄清石灰水时,溶液变浑浊。由此可以确定原混合气体中:一定含有______ _____________________;可能含有_________________;一定不含________________(填化学式)。
26.(本题共4分)
下列事实不能用勒夏特列原理解释的有_____________。
A.实验室制取氯气时,常用饱和食盐水除去混在氯气中的氯化氢气体
B.2SO2+O2 2SO3反应中,常鼓入过量的空气提高SO2的转化率
2SO3反应中,常鼓入过量的空气提高SO2的转化率
C.高压有利于合成氨的反应
D.升温至500℃左右,比室温时更有利于合成氨的反应
E.加入催化剂以增大合成氨反应速率
F.降低压强NO2的颜色先变浅后变深
G.可乐饮料瓶打开后会逸出气体
25.(本题共4分)
配平下列化学方程式,将化学计量数填在相应横线上。
(1)______NH3+______NO2=______N2+______H2O
(2)_______Zn+_____HNO3=_____Zn(NO3)2+_____NH4NO3+_____H2O
24.已知反应:KClO3+6HCl=KCl+3Cl2↑+3H2O,若用K35ClO3与H37Cl作用,下列说法正确的是 ( )
A.此反应中,每生成3 mol Cl2转移电子6 mol
B.生成物KCl中只含有37Cl
C.生成的Cl2中只含有35Cl
D.生成Cl2的相对分子质量为72
|
卷Ⅱ(非选择题 共40分)
23.下列四组实验中,根据实验事实得出的结论,正确的是 ( )
A.实验:在未知试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加硝酸不溶解。结论:原未知试液一定含有SO42-
B.实验:在未知试液中加NaOH溶液并加热得无色刺激性气体,该气体能使紫色石蕊试液变蓝。结论:原未知试液一定含有NH4+
C.实验:某未知气体在空气中燃烧,其产物能使无水CuSO4粉末变蓝色。结论:原气体一定是氢气
D.实验:在未知试液中滴加HCl溶液得无色气体,将该气体通入过量澄清石灰水中得白色沉淀。结论:原未知试液一定有CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com