
题目列表(包括答案和解析)
9.在一定温度和压强下,将一容积15ml的试管充满NO2后,倒置于一个盛水的水槽中。当试管内液面上升至一定高度不再变化时,在相同条件下再通入O2,若要使试管内液面仍保持在原高度,则应通入O2体积为( )
A.3.75ml B.7.5ml C.8.75ml D.10.5ml
8、可逆反应aA+bB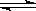 cC+dD+Q,(A、B、C、D都是气体)如图所示,下列叙述正确的( )
cC+dD+Q,(A、B、C、D都是气体)如图所示,下列叙述正确的( )
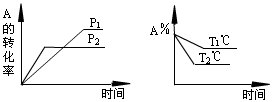
A.p1<p2,a+b<c+d,T1℃<T2℃,Q为负值
B.p1>p2,a+b>c+d,T1℃>T2℃,Q为正值
C.p1<p2,a+b<c+d,T1℃>T2℃,Q为正值
D.以上答案均不对
7.某温度下,在体积为5 L的密闭容器中,充入1 mol A气体,发生如下可逆反应:2A(g) B(g)+C(g);ΔH=+
B(g)+C(g);ΔH=+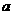 kJ·mol-1 (a>0),2 min后反应达到平衡,A为0.4 mol。下列叙述中不正确的是
kJ·mol-1 (a>0),2 min后反应达到平衡,A为0.4 mol。下列叙述中不正确的是
A.0~2 min时间内B物质的平均反应速率为0.03 mol/(L·min)
B.充分反应后,反应吸收的热量小于0.5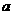 kJ
kJ
C.达平衡后,保持温度和容器体积不变,再充入1 mol A,平衡向正反应方向移动
D.若温度和容器体积不变,起始时充入B和C各0.5 mol,则达平衡时,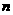 (A)等于0.4 mol
(A)等于0.4 mol
6.下列说法正确的是 ( )
A.pH=2与pH=1的硝酸中c(H+)之比为1:10
B.H2CO3溶液中c(H+)与c(CO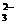 )之比为2:1
)之比为2:1
C.0.2mol/L与0.1mol/L醋酸中c(H+)之比为2:1
D.NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1
5.在无色强酸性溶液中,下列各组离子能大量共存的是( )
A.Na+ 、Fe2+、MnO4-、Cl- B.K+、Fe3+、SCN-、SO42-
C.NH4+、Ca2+、Cl-、NO3- D.Cu2+、Al3+、Cl-、OH-
4、一定条件下,可逆反应N2 +3H2 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是(
)
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是(
)
A、加催化剂,V正、V逆 都发生变化,且变化的倍数相等
B、加压,V正、V逆 都增大,且V正 增大的倍数大于V逆 增大的倍数
C、降温,V正、V逆 都减小,且V正 减小的倍数大于V逆 减小的倍数
D、增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数
3.已知三角锥形分子E和直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10)如下图,则下列判断错误的是( )

A.G是最活泼的非金属单质 B.L是极性分子
C.E能使紫色石蕊试液变蓝色 D.M化学性质活泼
2.对于反应2A(g)+3B(g)=C(g)+5D(g),在某段时间内的平均反应速率为 ,(x代表某反应物或生成物)之间的关系,正确的是( )
,(x代表某反应物或生成物)之间的关系,正确的是( )
A. B.
B.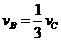 C.
C.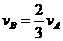 D.
D.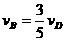
1.近年光化学烟雾问题已引起人们的注意,造成光化学烟雾的主要物质是( )A.二氧化硫 B.二氧化氮 C.氨气 D.一氧化碳
21.(9分)重晶石(BaSO4)难溶于水,要转变为BaCO3再制备其他钡盐。工业上一般采用高温煅烧还原法;实验室可以采用沉淀转化法。
Ⅰ.高温煅烧还原法:

(1)煅烧还原的热化学方程式为 。
有关的数据:Ba(s)+S(s)+2O2(g)=BaSO4(s) △H=-1473.2 kJ/mol
C(s)+ O2(g)=CO(g) △H=-110.5
kJ/mol
O2(g)=CO(g) △H=-110.5
kJ/mol
Ba(s)+S(s)=BaS(s) △H=-460 kJ/mol
(2)经检验BaS的水溶液呈碱性,原因是(用离子方程式表示) 。
Ⅱ.沉淀转化法:
向BaSO4沉淀中加入饱和Na2CO3溶液,充分搅拌,弃去上层清液。如此处理多次,直到BaSO4全部转化为BaCO3;BaSO4(s)+CO32-(aq) BaCO3(s)+SO42-(aq)(该反应的平衡常数K=0.042)。
BaCO3(s)+SO42-(aq)(该反应的平衡常数K=0.042)。
(3)现有0.20mol BaSO4,每次用1.00L 2.0 mol/L饱和Na2CO3溶液处理,假定BaSO4能全部转化,至少需要处理几次?(写出计算过程)
(4)从“绿色化学”角度分析,用饱和Na2CO3溶液沉淀转化法的优点是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com