
题目列表(包括答案和解析)
5. 把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;b、c相连时,c上有大量气泡;b、d相连时,d上有大量气泡产生,则这四种金属的活动顺序由强到弱为
A.a > b > c > d B.a > c > b > d
C.c > a > b > d D.b > d > c > a
4. 下列变化是因原电池反应而引起的是
A.在空气中金属铝表面迅速氧化形成保护膜
B.常温下,铁被浓硫酸“钝化”形成保护膜
C.在潮湿的空气中钢铁易生锈
D.在潮湿的空气中过氧化钠易变质
3. 把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是
A.盐酸的浓度 B.铝条的表面积
C.溶液的温度 D.加少量Na2SO4
2.已知化学反应C(s)+O2(g)  CO2(g)
是放热反应。据此推断下列说法正确的是
CO2(g)
是放热反应。据此推断下列说法正确的是
A.反应物的总能量大于生成物的总能量
B.反应物的总能量小于生成物的总能量
C.反应物的总能量等于生成物的总能量
D.无法确定反应物总能量和生成物总能量的相对大小
1.下列反应既属于氧化还原反应,又是吸热反应的是
A.锌粒与稀硫酸的反应
B.灼热的木炭与CO2的反应
C.Ba(OH)2•8H2O晶体与NH4Cl晶体的反应
D. 甲烷在空气中燃烧的反应
15. 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位用kJ•mol-1表示。请认真观察下图,然后回答问题。
(1)图中反应是 (填“吸热”或“放热”)反应,该反应 (填“需要”或“不需要”)提供能量,该反应的△H=
(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+1/2O2(g) === H2O(g) △H=-241.8kJ•mol-1,该反应的活化能为167.2 kJ•mol-1,则其逆反应的活化能为 。
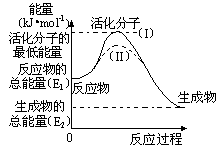 (3)对于同一反应,图中虚线(II)与实线(I)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是
。
(3)对于同一反应,图中虚线(II)与实线(I)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是
。
14. 依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________________________________________。
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量
_______________________________________________________________。
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________
13. 在一定条件下A与B反应可生成C和D,其能量变化如图:
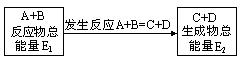
(1)下列有关反应A+B===C+D的说法正确的是 。
A. 反应前后原子的种类和数目一定不变
B. 该反应若有能量变化,则一定是氧化还原反应
C. 该反应若为放热反应,则不需加热反应就一定能自发进行
D. 反应物的总质量与生成物的总质量一定相等,且遵循能量守恒
(2)若E1<E2,则生成物的总能量 (填“>”、“<”或“=”)反应物的总能量,为 (填“吸热”或“放热”)反应。
15. 发射卫星时可用肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知:N2(g)+2O2(g) ==2NO2(g) ΔH=+67.7 kJ•mol-1
N2H4(g)+O2(g)== N2(g)+2H2O(g) ΔH=-534 kJ•mol-1
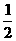 H2(g)+
H2(g)+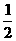 F2(g)== HF(g) ΔH=-269 kJ•mol-1
F2(g)== HF(g) ΔH=-269 kJ•mol-1
H2(g)+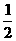 O2(g) == H2O(g) ΔH=-242 kJ•mol-1
O2(g) == H2O(g) ΔH=-242 kJ•mol-1
(1)肼和二氧化氮反应的热化学方程式为 。
(2)有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,肼和氟反应的热化学方程式为 。
14. 已知:2Al (s)+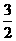 O2(g)=== Al2O3(s) △H= -1 644.3 kJ•
mol-1
O2(g)=== Al2O3(s) △H= -1 644.3 kJ•
mol-1
2Fe (s) +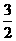 O2(g)=== Fe2O3(s) △H= -815.88 kJ•
mol-1
O2(g)=== Fe2O3(s) △H= -815.88 kJ•
mol-1
试写出铝粉与氧化铁粉末发生铝热反应的热化学方程式___________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com