
题目列表(包括答案和解析)
9. 0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量,又知:H2O (l ) == H2O(g) △H = +44 kJ·mol-1,下列热化学方程式,正确的是( )
A. 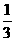 B2H6 (g)+O2 (g) ==
B2H6 (g)+O2 (g) == 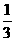 B2O3 (g)+H2O (g) △H = -677.7 kJ·mol-1
B2O3 (g)+H2O (g) △H = -677.7 kJ·mol-1
B. B2H6 (g)+3O2 (g) == B2O3(s)+3H2O (g) △H = -2165 kJ·mol-1
C. B2H6 (g)+3O2 (g) == B2O3(s)+3H2O (g) △H = -2033 kJ·mol-1
D. B2H6 (g)+3O2 (g) == B2O3(s)+3H2O(l) △H = -2033 kJ·mol-1
8. 已知25℃、101kPa条件下:4Al (s) + 3O2 (g) == 2Al2O3 (s) △H = -2834.9 kJ·mol-1
4Al (s) +2O3 (g) == 2Al2O3 (s) △H = -3119.91 kJ·mol-1
由此得出的结论正确的是( )
A.等质量的O2比O3能量低,由O2变O3 为吸热反应
B.等质量的O2比O3能量低,由O2变O3 为放热反应
C.O3比O2稳定,由O2变O3 为吸热反应
D.O2比O3稳定,由O2变O3 为放热反应
7. 如下图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是( )
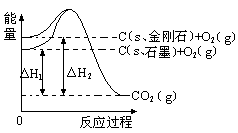
A. C(s、石墨)== C(s、金刚石) △H= +1.9 kJ•mol-1
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
6. 甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量,则下列热化学方程式中正确的是 ( )
A. 2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l) ΔH= +890 kJ·mol-1
B. CH4(g) + 2O2(g) == CO2(g) +2H2O(l) ΔH= +890 kJ·mol-1
C. CH4(g) + 2O2(g) == CO2(g) +2H2O(l) ΔH= -890 kJ·mol-1
D. 2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l) ΔH= -890 kJ·mol-1
5. 灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s,白)+2HCl(aq)== SnCl2(aq)+H2(g) ΔH1
②Sn(s,灰)+2HCl(aq)== SnCl2(aq)+H2(g) ΔH2
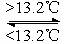
③Sn(s,灰) Sn(s,白) ΔH3 = +2.1 kJ·mol-1
下列说法正确的是( )
A.ΔH1>ΔH2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏
4. 1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,此反应的热化学方程式为( )
A.C + H2O == CO + H2 ΔH= +131.3 kJ·mol-1
B. C(s)+ H2O(g) == CO(g) + H2(g) ΔH= +10.94 kJ·mol-1
C. C(s)+ H2O(l) == CO(g) + H2(g) ΔH= +131.3 kJ·mol-1
D. C(s)+ H2O(g) == CO(g) + H2(g) ΔH= +131.3 kJ·mol-1
3. 下列说法正确的是( )
A. 化学反应除了生成新的物质外,还伴随着能量的变化
B. 据能量守恒定律,反应物的总能量一定等于生成物的总能量
C. 放热的化学反应不需要加热就能发生
D. 吸热反应不加热就不会发生
2. 已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO4•5H2O(s) === CuSO4(s)+5H2O(l) △H=+Q2 kJ·mol-1则Q1、Q2的关系为 ( )
A. Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
1. 下列选项中说明乙醇作为燃料的优点的是 ( )
①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种再生能源 ④燃烧时放出大量热量
A. ①②③ B. ①②④ C. ①③④ D. ②③④
18.(12分)将气体A、B置于容积为2L的密闭容器中,发生如下反应:4A(g) +B(g) 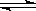 2C(g)
,反应进行到4s末,测得A的物质的量为0.5mol,B的物质的量为0.4mol,C的物质的量为0.2mol,则:
2C(g)
,反应进行到4s末,测得A的物质的量为0.5mol,B的物质的量为0.4mol,C的物质的量为0.2mol,则:
(1)用生成物C的浓度增加来表示该反应的速率为: ;
(2)用生成物A的浓度减少来表示该反应的速率为: ;
(3)反应前A、B的物质的量浓度分别是: 、 。
人教版必修2第二章《化学反应与能量》测试题(A卷)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com