
题目列表(包括答案和解析)
19.(8分)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出该反应的热化学方程式__________________________________________。
(2)已知H2O(l)====H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知N2(g)+2O2(g)====2 NO2(g);△H=+67.7 kJ·mol-1, N2H4(g)+O2(g)=== N2(g)+2H2O (g);△H=-534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式________________________________________。
18. 已知热化学方程式:
① C2H2(g) +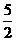 O2(g)
== 2CO2(g)+H2O(l) ΔH1=-1301.0
kJ•mol-1
O2(g)
== 2CO2(g)+H2O(l) ΔH1=-1301.0
kJ•mol-1
② C(s)+ O2(g) == CO2(g) △H2=-393.5 kJ•mol-1
③ H2(g)+ O2(g) == H2O(1) △H3 = -285.8 kJ·mol-1
则反应④ 2C(s)+ H2(g) == C2H2(g)的△H为( )
A. +228.2 kJ·mol-1 B. -228.2 kJ·mol-1 C. +1301.0 kJ·mol-1 D. +621.7 kJ·mol-1
17. 已知
(1)H2O(g) == H2O(l) ΔH1=-Q1 kJ·mol-1
(2)CH3OH(g) == CH3OH(l) △H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) == 2CO2(g)+4H2O(g) △H3=-Q3 kJ·mol-1
(Q1、Q2、Q3均大于0)若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ) ( )
A. Q1+Q2+Q3 B. 0.5 Q3-Q2+2Q1 C. 0.5 Q3+ Q2-2Q1 D. 0.5(Q1+Q2+Q3)
16. 已知热化学方程式:
H2O(g) == H2(g) + O2(g) △H = +241.8 kJ·mol-1
H2(g)+ O2(g) == H2O(1) △H = -285.8 kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88kJ B. 吸热2.44 kJ C.放热44kJ D. 吸热44 kJ
15. 已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g) == 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
(2)C(s)+ O2(g) == CO2(g) △H2=-393.5 kJ•mol-1
(3)H2(g) +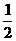 O2(g) == H2O(l) △H3=-285.8kJ·mol-1
O2(g) == H2O(l) △H3=-285.8kJ·mol-1
则反应2 C(s)+2H2(g) +O2(g) == CH3COOH(l)的△H为( )
A. -488.3 kJ·mol-1 B.-244.15 kJ·mol-1 C.+488.3 kJ·mol-1 D.+244.15 kJ·mol-1
14. 已知:
CH3CH2CH2CH3(g)+6.5O2(g) == 4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1
(CH3)2CHCH3(g)+6.5O2(g) == 4CO2(g)+5H2O(l) ΔH=-2 869kJ·mol-1
下列说法正确的是( )
A. 正丁烷分子储存的能量大于异丁烷分子
B. 正丁烷的稳定性大于异丁烷
C. 异丁烷转化为正丁烷的过程是一个放热过程
D. 异丁烷分子中的碳氢键比正丁烷的多
13. 已知:CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH=- Q1 ;
2H2(g)+O2(g) == 2H2O(g) ΔH=- Q2;
H2O(g) == H2O(l) ΔH=- Q3
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为( )
A. 4Q1+0.5Q2 B. 4Q1+Q2+10Q3 C. 4Q1+2Q2 D. 4Q1+0.5Q2+9Q3
12. 已知下列两个热化学方程式
2H2(g) + O2(g) == 2H2O(l) △H =-571.6kJ·mol-1
C3H8(g) +5O2(g) == 3CO2(g) + 4H2O(l) △H =-2 220.0kJ·mol-1
实验测得氢气和丙烷的混和气体共5 mol完全燃烧时放热3847kJ,则混和气体中氢气与丙烷的体积比是 ( )
A. 1:3 B. 3:1 C. 1:4 D. 1:1
11. 强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) ⊿H=-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应⊿H1、⊿H2、⊿H3的关系正确的是( )
A.⊿H1>⊿H2>⊿H3 B.⊿H1<⊿H3<⊿H2
C.⊿H1<⊿H2<⊿H3 D.⊿H1>⊿H3>⊿H2
10. 2007年3月,温家宝指出“优化结构、提高效益和降低消耗、保护环境”,这是我国国民经济和社会发展的基础性要求。你认为下列行为不符合这个要求的是( )
A. 大力发展农村沼气,将废弃的秸轩转化为清洁高效的能源
B. 加快太阳能、风能、生物质能、海洋能等清洁能源的开发利用
C. 研制开发以水代替有机溶剂的化工涂料
D. 将煤转化成气体燃料可以有效地减少“温室效应”的气体产生
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com