
题目列表(包括答案和解析)
24.图3是铜锌原电池装置。其电池的总反应是:Zn(s) + CuSO4(aq)== ZnSO4(aq) + Cu(s)。

请回答以下问题:
⑴R的名称是____________,其作用是____________________________________。R中的阳离子移向_______(填A或B)中的溶液。
⑵电极Y的材料是________,B中的电解质溶液是________________。
⑶X为原电池的______极,其电极反应式是____________________________。
23.向盛有1 mL 0.1 mol/L MgCl2溶液的试管中滴加1-2滴2 mol/L NaOH溶液,观察到有白色沉淀生成,该反应的离子方程式是______________________________。再滴加2滴0.1 mol/L FeCl3溶液,观察到白色沉淀转化为红褐色沉淀,该反应的离子方程式是____________________________________________。由以上现象可以推知,相同条件下Mg(OH)2和Fe(OH)3中溶解度较大的是_________________。
22.⑴常温下,0.10 mol/L NH4Cl溶液pH____7(填>、=、<),溶液中各离子浓度由大到小的顺序是______________________________。
⑵相同物质的量浓度的Na2S溶液与NaHS溶液,pH大小: Na2S____NaHS(填>、=、<),两种溶液中微粒种类:Na2S_______NaHS(填>、=、<)。
⑶NaHCO3溶液呈碱性的原因是________________________________(写出有关的离子方程式,下同),Al2(SO4)3溶液呈酸性的原因是________________________________,将NaHCO3溶液跟Al2(SO4)3溶液混合,现象是___________________________,相关反应的离子方程式是________________________________
21、由氢气和氧气反应生成1mol水蒸气放热241.8KJ,写出该反应的热化学方程式
_______________________
若1 g水蒸气转化成液态水时放热2.444 kJ,则反应H2(g) + 1/2O2(g) == H2O(l)的
△H =
kJ· 。
。
20、在下图各烧杯中盛有海水,铁在其中腐蚀速率由快到慢的顺序是( )。
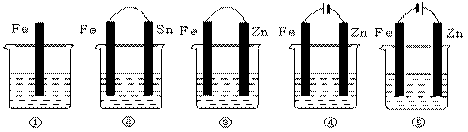
A.①>②>③>④>⑤ B.⑤>④>③>②>①
C.④>②>①>③>⑤ D.②>③>⑤>①>④
19.已知0.02 mol·L-1CH3COOH溶液和0.01 mol·L-1NaOH溶液以等体积混和后溶液呈酸性,则该混合液中微粒浓度关系正确的( )。
A.c (CH3COO-)>c (Na+)
B.c (Na+) + c (H+) =c (OH-) +c (CH3COOH)+c (CH3COO-)
C.c (CH3COOH)>c (CH3COO-) D.c (CH3COOH)+c (CH3COO-)=0.02 mol·L-1
18、据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为: 2CH3OH + 3O2
+ 4OH-  2CO32- + 6H2O,则下列说法正确的是 ( )。
2CO32- + 6H2O,则下列说法正确的是 ( )。
A.构成该电池的正极和负极必须是两种活性不同的金属
B.充电时有CH3OH生成的电极为阳极
C.放电时电解质溶液的pH逐渐增大
D.放电时负极的电极反应为:CH3OH-6e- +8OH- = CO32- + 6H2O
17.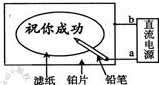 某学生设计了一个“黑笔写红字”的趣味实验滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此下列叙述正确的是( )。
某学生设计了一个“黑笔写红字”的趣味实验滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此下列叙述正确的是( )。
A.铅笔芯作阳极,发生还原反应
B.铂片作阴极,发生氧化反应
C.铅笔尖附近有少量的氯气产生
D.红字是H+放电,破坏了水的电离平衡,c(OH-)增大造成
16.用某浓度的HCl溶液滴定某浓度的NaOH溶液25.00 mL,滴定曲线如图2所示。则HCl溶液与NaOH溶液的物质的量浓度可能是 (单位:mol·L-1)

|
|
A |
B |
C |
D |
|
HCl |
0.12 |
0.10 |
0.10 |
0.08 |
|
NaOH |
0.10 |
0.12 |
0.08 |
0.10 |
15、250 ℃和1.01×105 Pa时,反应 2N2O5(g)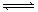 4NO2(g)+O2(g) △H=+56.76 kJ/mol,
4NO2(g)+O2(g) △H=+56.76 kJ/mol,
自发进行的原因是( )。
A.是吸热反应 B.是放热反应;
C.是熵减少的反应 D.熵增大效应大于能量效应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com