
题目列表(包括答案和解析)
26.(5分)碘是人体中不可缺少的 (选填“常量”或“微量”)元素。
食盐中加入碘元素能有效防止缺碘引起的疾病。以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%。现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%
(1)、食盐中加入碘化钾的碘损失率高的原因是 ;
(2)、萃取碘水中的碘时,一般选用的试剂是(填字母) ;
A、酒精 B、四氯化碳 C、乙酸
(3)、可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾。反应的化学方程式为:
5KI+KIO3 + 6HCl == 6KCl + 3I2 + 3H2O,反应的现象是 ;
(4)、已知碘酸钾受热易分解,你认为在用碘酸钾加碘盐进行烹饪时应注意什么问题?
25.(5分)(2)淀粉的化学式是: ;药品生产常选用淀粉作填充剂、粘合剂。服用添加淀粉的药物不会伤害身体的原因是 。
青霉素是医学上一种常用的抗生素,在体内经酸性水解后得到青霉氨基酸其结构简式为:
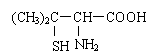
请写出青霉氨基酸可能具有的一种化学性质 。
;油脂在人体内通过水解生成 和甘油,在氧化分解,为人体提供能量。人体摄入的蛋白质在胃蛋白酶和胰蛋白酶的作用下,水解成 。
24.(5分)实验证明维生素C能使酸性高锰酸钾溶液褪色,也能使滴有KSCN溶液的氯化铁溶液红色褪去, 证明维生素C具有 性。维生素C也能使滴有淀粉溶液的碘液 。葡萄糖水能发生银镜反应,说明葡萄糖有 性,它也能使 悬浊液产生砖红色沉淀. 人体血红蛋白中含有Fe2+,如果误食亚硝酸盐会使人中毒,因为亚硝酸盐会使Fe2+转变成Fe3+,生成高铁血红蛋白而丧失与O2结合的能力。服用 可缓解亚硝酸盐的中毒,
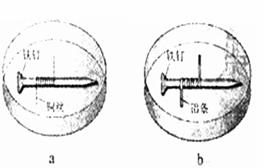
23.如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是
A、a中铁钉附近呈现红色
B、b中铁钉上发生还原反应
C、a中铜丝上发生氧化反应
D、b中铝条附近有气泡产生
22.对于反应2SO2(g)+O2(g) 2SO3(g)能增大正反应速率的措施是
2SO3(g)能增大正反应速率的措施是
A.通入大量O2 B.增大容器容积
C.移去部分SO3 D.降低体系温度
21.下列关于Cl、N、S等非金属元素化合物的说法正确的是
A.漂白粉的成分是次氯酸钙
B.实验室可用浓硫酸干燥氨气
C.实验室可用NaOH 处理NO2 和HCl 废气
D.Al2(SO4)3 可除去碱性废水及酸性废水中的悬浮颗粒
20.根据陈述的知识,类推得出的结论正确的是
A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O
B.乙烯可使酸性高锰酸钾溶液褪色,则丙烯也可以使其褪色
C.CO2和SiO2 化学式相似,则CO2与SiO2的物理性质也相似
D.金刚石的硬度大,则C60的硬度也大
19.氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛应用于电子陶瓷等工业领域。
在一定条件下,AlN可通过反应:Al2O3+N2+3C
 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮的化合价为+3
D.AlN的摩尔质量为41 g
18.从绿色化学的理念出发,下列实验不宜用图7所示装置进行的是
A.不同浓度的硝酸与铜的反应
B.稀硫酸与纯碱或小苏打反应
C.铝与氢氧化钠溶液或稀盐酸反应
D.H2O2在不同催化剂作用下分解
17.下列反应的离子方程式正确的是
A.钠与水反应:Na+H2O=Na++OH-+H2↑
B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
C.氢氧化铝中和胃酸:Al(OH)3+H+=Al3++3H2O
 D用氯化铁溶液腐蚀电路板:Fe3++Cu=Fe2++Cu2+
D用氯化铁溶液腐蚀电路板:Fe3++Cu=Fe2++Cu2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com