
题目列表(包括答案和解析)
6.(8分)某校化学小组学生利用下图所列装置进行“铁与水反应”的实验。(图中夹持及尾气处理装置均已略去)
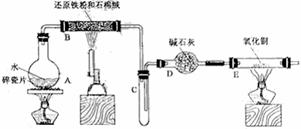
(1)仪器A的名称是 。
(2)仪器B中发生反应的化学方程式是 。
(3)仪器E中的现象是黑色固体变红,右端管壁有水珠。设置该反应的目的是
。
(4)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:
。
选答题(共20分)
其中第7、8、9题为《化学与生活》模块题,第10、11、12题为《化学反应原理》模块题,第13、14、15题为《有机化学基础》模块题。考生只能从三个模块中任选一个作答,不得跨模块答题,否则只能以所答的第一个模块计分。
《化学与生活》模块
5.(8分)已知X、Y、Z为三种短周期元素,其中X的原子核中只有1个质子,X与Y原子的最外层电子数之和等于Z原子的最外层电子数,Z的-2价离子的电子层结构与氖的相同。
现有A、B、C、D、E五种中学化学中常见的化合物,转化关系如下所示。
A → B→ C → D → E
涉及反应的所有反应物和产物均由X、Y、Z中的一种或几种元素组成。请回答:
(1)D的浓溶液能使蛋白质显黄色,由此可知D的化学式为__________________。
(2)E是一种离子化合物。在实验室中检验该物质所含阳离子的实验操作方法和现象为:取少量E放入试管中,加入少量NaOH溶液并加热,________________________
____________________________________________________________________。
(3)A生成B的反应是工业制取D的基础,该反应的化学方程式为___________________________________________。在反应中若有1.25 mol 电子发生转移,则参加反应的A的体积为 L(标准状况)。
4.(4分)为除去粗盐中的少量Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
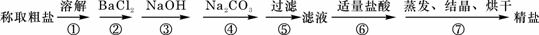
(1)加入过量BaCl2溶液的目的是除去粗盐中的 ____________(填化学式)。
(2)第③步的目的是除去粗盐中的Mg2+,反应的离子方程式为___________________。
3.(4分)(1)自然界中的大多数金属以 形式存在,少数不活泼的金属如金等能以单质的形式存在。
(2)自然界中的铁矿石主要有磁铁矿和赤铁矿,赤铁矿主要成分的化学式为 。
(3)海水中溴的藏量丰富,约占地球溴总藏量的99%,故溴有“海洋元素”之称。溴的一种工业提取方法为,将氯气通入到富含溴离子的海水中,使溴置换出来,再利用单质溴在水中和其他溶剂中溶解度的不同提纯溴。该操作方法称为 ,用到的主要实验仪器名称是 。
2.(3分)在①乙烯、②苯、③乙酸三种物质中,能与硝酸发生取代反应的是 (填序号,下同),能与Br2发生加成反应的是 ,能发生酯化反应的是 。
1.
 (3分)明代宋应星所著《天工开物》记载的炼锡方法基本上就是现代用的碳还原法,该反应的化学方程式为:SnO2 +
2C Sn + 2CO ↑。反应中,作为氧化剂的物质是
(填化学式),作为还原剂的物质是
(填化学式)。在该反应中,若消耗了1 mol SnO2,则生成
mol Sn。
(3分)明代宋应星所著《天工开物》记载的炼锡方法基本上就是现代用的碳还原法,该反应的化学方程式为:SnO2 +
2C Sn + 2CO ↑。反应中,作为氧化剂的物质是
(填化学式),作为还原剂的物质是
(填化学式)。在该反应中,若消耗了1 mol SnO2,则生成
mol Sn。
25.下列实验中,有白色沉淀产生且最终不会消失的是( )
A.向FeCl2溶液中逐滴滴入NaOH溶液
B.向硝酸银溶液中逐滴滴入氨水,直至过量
C.向澄清石灰水中通入二氧化碳,直至过量
D.向AlCl3溶液中逐滴滴入氨水,直至过量
第Ⅱ卷(非选择题 共50分)
必答题(共30分)
24.下列离子方程式中,正确的是( )
A.铁和氯化铁溶液的反应:Fe + Fe3+ == 2Fe2+
B.大理石和稀盐酸的反应:CO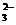 + 2 H+== CO2 ↑ + H2O
+ 2 H+== CO2 ↑ + H2O
C.碳酸氢钠溶液和氢氧化钠溶液反应:HCO + OH-== CO
+ OH-== CO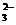 + H2O
+ H2O
D.铜和稀硝酸反应:Cu+H++NO =Cu2++NO↑十H2O
=Cu2++NO↑十H2O
23.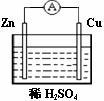 对于锌、铜和稀硫酸组成的原电池(如右图),下列有关说法
对于锌、铜和稀硫酸组成的原电池(如右图),下列有关说法
不正确的是( )
A.Zn是负极
B.负极上发生氧化反应
C.负极发生的反应是 Zn - 2e-
== 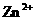
D.正极发生的反应是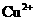 + 2e- == Cu
+ 2e- == Cu
22.下列叙述中,指定粒子的数目约为6.02×1023的是( )
A.1.6 g CH4中含有的电子数
B.1 mol/L的稀硫酸100 mL中含有H+的数目
C.24 g金属镁与足量的盐酸反应转移的电子数
D.标准状况下,22.4 L H2和CO混合气体中的原子数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com