
题目列表(包括答案和解析)
14. 对于mA(g) + nB(g) pC(g) + qD(g) 的平衡体系,当升高温度时,体系的平均相对摩尔质量从26变为29,则下列说法正确的是
对于mA(g) + nB(g) pC(g) + qD(g) 的平衡体系,当升高温度时,体系的平均相对摩尔质量从26变为29,则下列说法正确的是
A. m+n>p+q,正反应是放热反应 B. m+n>p+q,正反应是吸热反应
C. m+n<p+q,逆反应是放热反应 D. m+n<p+q,正反应是吸热反应
13.下列叙述正确的是
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
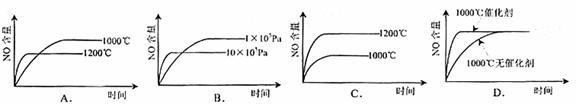
12.已知:4NH3(g)+5O2(g)
 4NO(g)+6H2(g) △H= - 1025kJ·mol-1
该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
4NO(g)+6H2(g) △H= - 1025kJ·mol-1
该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
11.己二酸是合成尼龙6,6的原料。据统计我国每年的需求量均在几十万吨以上。现有两种合成方法:
方法一(传统工艺):以苯为原料制备己二酸:

方法二(最新开发):以蔗糖为原料制备己二酸:

与传统工艺相比,关于方法二的优点,下列描述你认为正确的是:⑴原料(植物资源)来源广泛;⑵原料无毒无害;⑶反应在温和条件进行而不使用高压设备;⑷生产过程中对环境的危害小;⑸生产过程中只需要生物催化剂;⑹工艺简单,产率高。
A.⑴⑵⑷⑹ B.⑴⑵⑶⑸ C.⑴⑵⑶⑷⑹ D.全部
10.把a、b、c、d四块金属浸泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若a、b相连时,a为负极;c、d相连,d上有气体逸出;a、c相连时a极减轻;b、d相连时,b为正极。则四种金属的活动性顺序为
A.a>b>c>d B. a>c>b>d C.a>c>d>b D.b>d>c>a
9.如下图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中加入无水CaCl2,在(3)中加入NH4Cl晶体,(2)中不加其他任何物质,发现(1)中红棕色变深,(3)中红棕色变浅,下列叙述正确的是


A.CaCl2溶于水时放出热量 B.烧瓶(1)中气体的压强不变
C.NH4Cl溶于水时放出热量 D.烧瓶(3)中气体的压强增大
8. 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列关于说法正确的是
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列关于说法正确的是
A.MMF能溶于水
B.MMF能发生取代反应和消去反应
C.1mol MMF能与6 mol氢气发生加成反应
D.1mol MMF能与含3 mol NaOH的水溶液完全反应
7.在一定温度下,反应:2A(s)
+ 2B(g)  C(g) + D(g) 在恒容容器中进行,不能说明该反应已经达到平衡的是
C(g) + D(g) 在恒容容器中进行,不能说明该反应已经达到平衡的是
A.混合气的密度不再随时间而变化 B.容器内的压强不随时间而变化
C.A的质量不再改变 D.平衡混合气体的平均相对分子质量不再改变
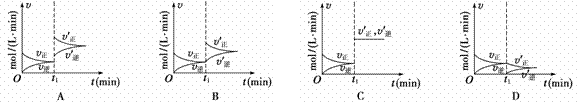
6. 可逆反应:2X(g)+ Y(s) 2Z(g) 在t1时刻达到平衡状态。当增大平衡体系压强时,下列有关正、逆反应速率(v)变化图象正确的是
可逆反应:2X(g)+ Y(s) 2Z(g) 在t1时刻达到平衡状态。当增大平衡体系压强时,下列有关正、逆反应速率(v)变化图象正确的是

5.已知反应:① 101kPa时, 2C(s) + O2(g) = 2CO(g) △H= - 221 kJ·mol-1
② 稀溶液中,H+(aq) + OH-(aq) =H2O(l) △H= - 57.3 kJ·mol-1
下列结论正确的是
A.碳的燃烧热大于 110.5 kJ·mol-1
B.① 的反应热为 221 kJ·mol-1
C.稀硫酸与稀NaOH 溶液反应的中和热为 - 57.3 kJ·mol-1
D.稀醋酸与稀NaOH 溶液反应生成1mol 水,放出57.3 kJ 热量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com