
题目列表(包括答案和解析)
28.(6分)I、II为两个极易导热的密闭容器,I保持容积不变,II中的活塞可上下移动,以保持内外压强相等。在相同条件下将3 mol A和1 mol B分别同时混合充入I、II两容器中,发生反应 3A(g) + B(g)  2C(g) + D(g)
2C(g) + D(g)
(1)达到平衡时,I中A的浓度为M mol/L,C的浓度为N mol/L,II中A的浓度为m mol/L,C的浓度为n mol/L,则M m;N n;(填>、<、=)
(2)保持温度不变,若向I中的平衡体系中再充入2 mol C和1 mol D,重新达到平衡后A的浓度为R mol/L。则( )
A. R = 2M B. R < M C. M < R < 2M D. R > 2M
27. (7分)(1)稀强酸、稀强碱反应生成1mol水时放出57.3 kJ的热。
① 实验室中可用稀盐酸和氢氧化钡稀溶液反应来测定中和热。请写出能表示该反应中和热的热化学方程式 ;
② 分别取100 mL 0.50 mol/L盐酸与100 mL 0.55 mol/L NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。假设盐酸和氢氧化钠溶液的密度都是1g/cm3,中和后生成溶液的比热容c = 4.18 J/(g·℃)。实验时,测得反应前盐酸与NaOH溶液的平均温度为21.5℃,反应后混合溶液的温度为24.9℃。
则实验测得的中和热△H=_______(保留1位小数)
③ 如果用含1 mol CH3COOH的稀醋酸与足量稀氢氧化钠溶液反应,反应放出的热____57.3 kJ(填“大于”、“小于”或“等于”);理由是_____________________________
(2)在催化剂的作用下CH4还原NO可以得到三种产物(该条件下均为气体),利用此反应能消除环境污染物NO。理论上每消耗标况下22.4 L NO就能放出290 kJ的热。写出该反应的热化学方程式
26. (6分)(1)CuCl2溶液有时呈黄色,有时呈绿色或蓝色,这是因为有CuCl2的水溶液中存在如下平衡:
[Cu(H2O)4]2+ +
4Cl-  [CuCl4]2- + 4H2O
[CuCl4]2- + 4H2O
蓝色 黄色
现欲使溶液由黄色变成蓝色,请写出一种可采用的方法:_____________________。
(2)在2SO2 + O2
 2SO3的平衡体系中,用由18O构成的氧气(18O2)替换掉一部分O2,平衡不发生移动。一段时间后SO2中18O的含量_________(填增加、减少或不变),其原因是__________。
2SO3的平衡体系中,用由18O构成的氧气(18O2)替换掉一部分O2,平衡不发生移动。一段时间后SO2中18O的含量_________(填增加、减少或不变),其原因是__________。
(3)在恒温恒容的两个密闭容器A和B中,分别加入 a mol 和 b mol 的HI(a > b),发生反应:2HI(g)  H2(g)
+ I2(g)达到平衡后。回答下列问题(用 “>”、“<” 或“=”填空):
H2(g)
+ I2(g)达到平衡后。回答下列问题(用 “>”、“<” 或“=”填空):
① 从反应开始到达到平衡所需要时间: tA _______ tB
② 平衡时的碘的浓度:cA(I2)______ cB(I2)
③ HI的平衡转化率:αA _______αB
25.工业上制备高纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)==Si(s)+4HCl(g) △H = +Q kJ/ mol(Q>0)
某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述中正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min)
D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应
24.一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)  3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是
A.2mol C B.2mol A、3mol B和1mol He(He不参加反应)
C.1mol B和1mol C D.2mol A、1mol B和3mol C
23.取c(H+)均为0.01 mol/L的盐酸和醋酸各100mL分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是
① 醋酸与锌反应放出氢气多 ② 盐酸和醋酸分别与锌反应放出的氢气一样多
③ 盐酸与锌反应放出氢气多 ④ 盐酸和醋酸分别与锌反应的速度一样大
⑤ 醋酸与锌反应速率大 ⑥ 盐酸与锌反应速率大
A.①⑥ B.②⑤ C.③④ D.①⑤
22.可逆反应aX+2Y(g)  2Z(g)在一定条件下的达到平衡后,t1和t2时各改变某一种外界条件,化学反应速率(v)-时间(t)图象如右图。则下列说法中正确的是
2Z(g)在一定条件下的达到平衡后,t1和t2时各改变某一种外界条件,化学反应速率(v)-时间(t)图象如右图。则下列说法中正确的是
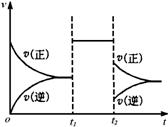 A.若X是固体,则t1时一定是增大了容器的压强
A.若X是固体,则t1时一定是增大了容器的压强
B.若X是气体,则t2时可能是增大了容器的压强
C.若X是固体,则t1时可能是增大了X的质量
D.t2时不可能是减小容器压强;若采用了降温措施,
则该反应的正反应方向△H<0
21.一定温度下,固定体积的容器中充入1 mol SO2和1 mol O2,再加入少量的NO,在体系中发生①2NO+O2=2NO2;②SO2+NO2=SO3+NO,下列说法中不正确的是
A.体系中的总反应是:2SO2+
O2  2SO3
2SO3
B.在反应过程中NO是催化剂
C.NO参与反应历程,降低反应活化能,加快反应速率
D.NO的引入可以增加SO2的平衡转化率
20.对于可逆反应:2A(g)+B(g)  2C(g) △H<0,下列各图中正确的是
2C(g) △H<0,下列各图中正确的是
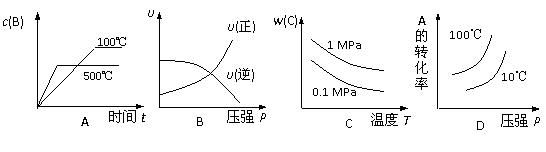

19.向容积为2 L的密闭容器中充入2 mol A和1 mol B,在一定条件下发生反应:
2A(g)+B(g) 3C(g)
3C(g)
经2 s达到平衡后,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2 mol·L-1
⑤其它条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
A.①②③ B.①③⑤ C.②④⑤ D.①③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com